Capacité thermique- c'est la quantité de chaleur absorbée par le corps lorsqu'il est chauffé de 1 degré.
La capacité thermique d'un corps est indiquée par un majuscule Lettre latine AVEC.
De quoi dépend la capacité thermique d’un corps ? Tout d’abord de par sa masse. Il est clair que chauffer, par exemple, 1 kilogramme d’eau nécessitera plus de chaleur que chauffer 200 grammes.
Qu’en est-il du type de substance ? Faisons une expérience. Prenons deux récipients identiques et versons de l'eau pesant 400 g dans l'un et dans l'autre - huile végétale pesant 400 g, commençons à les chauffer avec des brûleurs identiques. En observant les lectures du thermomètre, nous verrons que l'huile chauffe rapidement. Pour chauffer l’eau et l’huile à la même température, l’eau doit être chauffée plus longtemps. Mais plus nous chauffons l’eau longtemps, plus elle reçoit de chaleur du brûleur.
Ainsi, pour chauffer la même masse de substances différentes à la même température, il faut différentes quantités chaleur. La quantité de chaleur nécessaire pour chauffer un corps et, par conséquent, sa capacité thermique dépendent du type de substance qui compose le corps.
Ainsi, par exemple, pour augmenter la température d'une eau pesant 1 kg de 1°C, il faut une quantité de chaleur égale à 4200 J, et pour chauffer la même masse de 1°C huile de tournesol la quantité de chaleur nécessaire est de 1700 J.
Quantité physique montrant la quantité de chaleur nécessaire pour chauffer 1 kg d'une substance de 1 ºС est appelé la capacité thermique spécifique de cette substance.
Chaque substance possède sa propre capacité thermique spécifique, désignée par la lettre latine c et mesurée en joules par kilogramme degré (J/(kg °C)).
Chaleur spécifique la même substance dans différents états d'agrégation (solide, liquide et gazeux) est différente. Par exemple, la capacité thermique spécifique de l’eau est de 4 200 J/(kg °C) et la capacité thermique spécifique de la glace est de 2 100 J/(kg °C) ; l'aluminium à l'état solide a une capacité thermique spécifique de 920 J/(kg - °C) et à l'état liquide - 1080 J/(kg - °C).
Notez que l’eau a une capacité thermique spécifique très élevée. Par conséquent, l'eau des mers et des océans, se réchauffant en été, absorbe de l'air un grand nombre de chaleur. Grâce à cela, dans les endroits situés à proximité de grands plans d'eau, l'été n'est pas aussi chaud que dans les endroits éloignés de l'eau.
Calcul de la quantité de chaleur nécessaire pour chauffer un corps ou dégagée par celui-ci lors du refroidissement.
De ce qui précède, il ressort clairement que la quantité de chaleur nécessaire pour chauffer un corps dépend du type de substance qui le compose (c'est-à-dire sa capacité thermique spécifique) et de la masse du corps. Il est également clair que la quantité de chaleur dépend du degré d’augmentation de la température corporelle.
Ainsi, pour déterminer la quantité de chaleur nécessaire pour chauffer un corps ou dégagée par celui-ci lors du refroidissement, il faut multiplier la capacité thermique spécifique du corps par sa masse et par la différence entre ses températures finale et initiale :
Q= cm (t 2 -t 1),
Où Q- quantité de chaleur, c- la capacité thermique spécifique, m- masse corporelle, t1- température initiale, t 2- température finale.
Quand le corps se réchauffe t 2> t1 et donc Q >0 . Quand le corps se refroidit t 2i< t1 et donc Q< 0 .
Si la capacité thermique de tout le corps est connue AVEC, Q déterminé par la formule : Q = C (t 2 - t1).
22) Fusion : définition, calcul de la quantité de chaleur pour la fusion ou la solidification, chaleur spécifique de fusion, graphique de t 0 (Q).
Thermodynamique
Branche de la physique moléculaire qui étudie le transfert d'énergie, les modèles de transformation d'un type d'énergie en un autre. Contrairement à la théorie de la cinétique moléculaire, la thermodynamique ne prend pas en compte structure interne substances et microparamètres.
Système thermodynamique
C'est un ensemble de corps qui échangent de l'énergie (sous forme de travail ou de chaleur) entre eux ou avec environnement. Par exemple, l'eau dans la bouilloire refroidit et la chaleur est échangée entre l'eau et la bouilloire et la chaleur de la bouilloire avec l'environnement. Un cylindre avec du gaz sous le piston : le piston effectue un travail, à la suite duquel le gaz reçoit de l'énergie et ses macroparamètres changent.
Quantité de chaleur
Ce énergie, que le système reçoit ou libère pendant le processus d'échange thermique. Désignée par le symbole Q, elle se mesure, comme toute énergie, en Joules.
En raison de divers processus d'échange de chaleur, l'énergie transférée est déterminée à sa manière.
Chauffage et refroidissement
Ce processus se caractérise par un changement de température du système. La quantité de chaleur est déterminée par la formule

Capacité thermique spécifique d'une substance avec mesuré par la quantité de chaleur nécessaire pour se réchauffer unités de masse de cette substance par 1K. Chauffer 1 kg de verre ou 1 kg d’eau nécessite différentes quantités d’énergie. La capacité thermique spécifique est une quantité connue, déjà calculée pour toutes les substances, voir la valeur dans les tableaux physiques ;
Capacité thermique de la substance C- c'est la quantité de chaleur nécessaire pour chauffer un corps sans tenir compte de sa masse par 1K.


Fusion et cristallisation
La fusion est le passage d'une substance de l'état solide à l'état liquide. La transition inverse est appelée cristallisation.
L'énergie dépensée pour la destruction réseau cristallin substances, déterminées par la formule


La chaleur spécifique de fusion est une valeur connue pour chaque substance ; voir la valeur dans les tableaux physiques.
Vaporisation (évaporation ou ébullition) et condensation
La vaporisation est le passage d'une substance d'un état liquide (solide) à un état gazeux. Le processus inverse est appelé condensation.


La chaleur spécifique de vaporisation est une valeur connue pour chaque substance ; voir la valeur dans les tableaux physiques.
La combustion
La quantité de chaleur dégagée lorsqu'une substance brûle


La chaleur spécifique de combustion est une valeur connue pour chaque substance ; voir la valeur dans les tableaux physiques.
Pour un système de corps fermé et adiabatiquement isolé, l’équation du bilan thermique est satisfaite. Somme algébrique les quantités de chaleur émises et reçues par tous les corps participant à l'échange thermique sont nulles :
Q 1 + Q 2 +...+ Q n =0
23) La structure des liquides. Couche de surface. Force de tension superficielle : exemples de manifestation, calcul, coefficient de tension superficielle.
De temps en temps, n’importe quelle molécule peut se déplacer vers un emplacement vacant à proximité. De tels sauts de liquides se produisent assez souvent ; par conséquent, les molécules ne sont pas liées à des centres spécifiques, comme dans les cristaux, et peuvent se déplacer dans tout le volume du liquide. Ceci explique la fluidité des liquides. En raison de la forte interaction entre des molécules proches, elles peuvent former des groupes ordonnés locaux (instables) contenant plusieurs molécules. Ce phénomène est appelé clôturer la commande(Fig. 3.5.1).
Le coefficient β est appelé coefficient de température de dilatation volumétrique . Ce coefficient pour les liquides est dix fois supérieur à celui pour les solides. Pour l'eau par exemple à une température de 20 °C β in ≈ 2 10 – 4 K – 1, pour l'acier β st ≈ 3,6 10 – 5 K – 1, pour le verre de quartz β kv ≈ 9 10 – 6 K - 1 .
La dilatation thermique de l’eau présente une anomalie intéressante et importante pour la vie sur Terre. À des températures inférieures à 4 °C, l'eau se dilate à mesure que la température diminue (β< 0). Максимум плотности ρ в = 10 3 кг/м 3 вода имеет при температуре 4 °С.
Lorsque l’eau gèle, elle se dilate, de sorte que la glace reste flottante à la surface d’une étendue d’eau gelée. La température de l’eau gelée sous la glace est de 0 °C. En plus couches denses La température de l'eau au fond du réservoir est d'environ 4 °C. Grâce à cela, la vie peut exister dans l’eau des réservoirs gelés.
La plupart fonctionnalité intéressante les liquides sont la présence Surface libre . Un liquide, contrairement aux gaz, ne remplit pas tout le volume du récipient dans lequel il est versé. Une interface se forme entre le liquide et le gaz (ou la vapeur), qui se trouve dans des conditions particulières par rapport au reste du liquide. Il convient de garder à l'esprit qu'en raison de la compressibilité extrêmement faible, la présence d'une couche superficielle plus dense est nécessaire. n'entraîne aucun changement notable dans le volume du liquide. Si une molécule se déplace de la surface vers le liquide, les forces d’interaction intermoléculaire effectueront un travail positif. Au contraire, afin de tirer un certain nombre de molécules des profondeurs du liquide vers la surface (c'est-à-dire augmenter la surface du liquide), les forces extérieures doivent effectuer un travail positif Δ UN externe, proportionnel au changement Δ S superficie :
On sait en mécanique que les états d’équilibre d’un système correspondent à la valeur minimale de son énergie potentielle. Il s'ensuit que la surface libre du liquide tend à réduire sa surface. Pour cette raison, une goutte libre de liquide prend une forme sphérique. Le liquide se comporte comme si des forces agissant tangentiellement à sa surface contractaient (tiraient) cette surface. Ces forces sont appelées forces de tension superficielle .
La présence de forces de tension superficielle fait ressembler la surface d'un liquide à un film élastique étiré, à la seule différence que les forces élastiques dans le film dépendent de sa surface (c'est-à-dire de la façon dont le film est déformé) et de la tension superficielle. les forces ne dépend pas sur la surface du liquide.
Certains liquides, comme l’eau savonneuse, ont la capacité de former de fines pellicules. Les bulles de savon bien connues ont une forme sphérique régulière, ce qui montre également l'effet des forces de tension superficielle. Si un cadre en fil de fer, dont l'un des côtés est mobile, est plongé dans une solution savonneuse, alors tout le cadre sera recouvert d'un film de liquide (Fig. 3.5.3).
Les forces de tension superficielle ont tendance à réduire la surface du film. Pour équilibrer le côté mobile du cadre, une force externe doit lui être appliquée si, sous l'influence d'une force, la barre transversale se déplace de Δ. X, alors le travail Δ sera effectué UN vn = F vnΔ X = Δ E p = σΔ S, où Δ S = 2LΔ X– augmentation de la surface des deux côtés du film de savon. Puisque les modules de forces et sont les mêmes, on peut écrire :
|
Ainsi, le coefficient de tension superficielle σ peut être défini comme module de la force de tension superficielle agissant par unité de longueur de la ligne délimitant la surface.
En raison de l'action des forces de tension superficielle dans les gouttes de liquide et à l'intérieur des bulles de savon, une surpression Δ apparaît p. Si vous coupez mentalement une goutte sphérique de rayon R. en deux moitiés, alors chacune d'elles doit être en équilibre sous l'action des forces de tension superficielle appliquées à la frontière coupée de longueur 2π R. et forces de surpression agissant sur la zone π R. 2 sections (Fig. 3.5.4). La condition d’équilibre s’écrit
Si ces forces sont supérieures aux forces d'interaction entre les molécules du liquide lui-même, alors le liquide mouille surface d'un solide. Dans ce cas, le liquide s'approche de la surface du solide selon un certain angle aigu θ, caractéristique d'un couple liquide-solide donné. L'angle θ s'appelle Angle de contact . Si les forces d'interaction entre les molécules liquides dépassent les forces de leur interaction avec des molécules solides, alors l'angle de contact θ s'avère obtus (Fig. 3.5.5). Dans ce cas, on dit que le liquide ne mouille pas surface d'un solide. À mouillage completθ = 0, à complètement non mouillantθ = 180°.
Phénomènes capillaires appelé montée ou descente de liquide dans des tubes de petit diamètre - capillaires. Les liquides mouillants montent dans les capillaires, les liquides non mouillants descendent.
En figue. 3.5.6 montre un tube capillaire d'un certain rayon r, descendu à l'extrémité inférieure dans un liquide mouillant de densité ρ. L'extrémité supérieure du capillaire est ouverte. La montée du liquide dans le capillaire se poursuit jusqu'à ce que la force de gravité agissant sur la colonne de liquide dans le capillaire devienne égale en ampleur à la résultante. F n forces de tension superficielle agissant le long de la limite de contact du liquide avec la surface du capillaire : F t = F n, où F t = mg = ρ hπ r 2 g, F n = σ2π r cosθ.
Cela implique:
Avec non-mouillage complet θ = 180°, cos θ = –1 et donc h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
L'eau mouille presque complètement la surface du verre propre. Au contraire, le mercure ne mouille pas complètement la surface du verre. Par conséquent, le niveau de mercure dans le capillaire en verre descend en dessous du niveau dans le récipient.
24) Vaporisation : définition, types (évaporation, ébullition), calcul de la quantité de chaleur pour la vaporisation et la condensation, chaleur spécifique de vaporisation.
Évaporation et condensation. Explication du phénomène d'évaporation basée sur des idées sur la structure moléculaire de la matière. Chaleur spécifique de vaporisation. Ses unités.
Le phénomène de transformation d’un liquide en vapeur est appelé vaporisation.
Évaporation - le processus de vaporisation se produisant à partir d'une surface ouverte.
Les molécules liquides se déplacent avec à des vitesses différentes. Si une molécule se retrouve à la surface d’un liquide, elle peut vaincre l’attraction des molécules voisines et s’envoler hors du liquide. Les molécules éjectées forment de la vapeur. Les molécules restantes du liquide changent de vitesse lors d'une collision. Dans le même temps, certaines molécules acquièrent une vitesse suffisante pour s'envoler hors du liquide. Ce processus se poursuit afin que les liquides s'évaporent lentement.
*Le taux d'évaporation dépend du type de liquide. Les liquides dont les molécules sont attirées avec moins de force s'évaporent plus rapidement.
*L'évaporation peut se produire à n'importe quelle température. Mais à des températures élevées, l'évaporation se produit plus rapidement .
*Le taux d'évaporation dépend de sa superficie.
*Avec le vent (flux d'air), l'évaporation se produit plus rapidement.
Lors de l'évaporation, l'énergie interne diminue, car Lors de l'évaporation, le liquide laisse des molécules rapides, donc vitesse moyenne les molécules restantes diminuent. Cela signifie que s’il n’y a pas d’afflux d’énergie extérieure, alors la température du liquide diminue.
 Le phénomène de transformation de la vapeur en liquide est appelé condensation.
Elle s'accompagne d'une libération d'énergie.
Le phénomène de transformation de la vapeur en liquide est appelé condensation.
Elle s'accompagne d'une libération d'énergie.
La condensation de la vapeur explique la formation des nuages. La vapeur d’eau qui s’élève au-dessus du sol forme des nuages dans les couches supérieures d’air froid, constitués de minuscules gouttes d’eau.
Chaleur spécifique de vaporisation - physique une valeur indiquant la quantité de chaleur nécessaire pour convertir un liquide pesant 1 kg en vapeur sans changer de température.
Oud. chaleur de vaporisation désigné par la lettre L et mesuré en J/kg
Oud. chaleur de vaporisation de l'eau : L=2,3×10 6 J/kg, alcool L=0,9×10 6
Quantité de chaleur nécessaire pour convertir un liquide en vapeur : Q = Lm
Comme on le sait, au cours de divers processus mécaniques, une modification de l'énergie mécanique se produit. Une mesure de la variation de l'énergie mécanique est le travail des forces appliquées au système :
Lors de l'échange thermique, une modification de l'énergie interne du corps se produit. Une mesure du changement d’énergie interne pendant le transfert de chaleur est la quantité de chaleur.
Quantité de chaleur est une mesure du changement d'énergie interne qu'un corps reçoit (ou abandonne) pendant le processus d'échange thermique.
Ainsi, le travail et la quantité de chaleur caractérisent le changement d’énergie, mais ne sont pas identiques à l’énergie. Ils ne caractérisent pas l'état du système lui-même, mais déterminent le processus de transition énergétique d'un type à un autre (d'un corps à un autre) lorsque l'état change et dépendent de manière significative de la nature du processus.
La principale différence entre le travail et la quantité de chaleur est que le travail caractérise le processus de modification de l'énergie interne d'un système, accompagné de la transformation de l'énergie d'un type à un autre (de mécanique à interne). La quantité de chaleur caractérise le processus de transfert d'énergie interne d'un corps à un autre (du plus chauffé au moins chauffé), non accompagné de transformations énergétiques.
L'expérience montre que la quantité de chaleur nécessaire pour chauffer un corps de masse m de température en température est calculée par la formule
où c est la capacité thermique spécifique de la substance ;
![]()
L'unité SI de capacité thermique spécifique est le joule par kilogramme Kelvin (J/(kg K)).
Chaleur spécifique c est numériquement égal à la quantité de chaleur qui doit être transmise à un corps pesant 1 kg pour le chauffer de 1 K.
Capacité thermique le corps est numériquement égal à la quantité de chaleur nécessaire pour modifier la température corporelle de 1 K :
![]()
L'unité SI de capacité thermique d'un corps est le joule par Kelvin (J/K).
Pour transformer un liquide en vapeur à température constante, il faut dépenser une quantité de chaleur
où L est la chaleur spécifique de vaporisation. Lorsque la vapeur se condense, la même quantité de chaleur est libérée.
730. Pourquoi l'eau est-elle utilisée pour refroidir certains mécanismes ?
L'eau a une capacité thermique spécifique élevée, ce qui facilite une bonne évacuation de la chaleur du mécanisme.
731. Dans quel cas faut-il dépenser plus d'énergie : pour chauffer un litre d'eau à 1 °C ou pour chauffer cent grammes d'eau à 1 °C ?
Pour chauffer un litre d’eau, plus la masse est grande, plus il faut dépenser d’énergie.
732. Des fourchettes en cupronickel et en argent de masse égale ont été plongées dans l'eau chaude. Recevront-ils la même quantité de chaleur de l’eau ?
Une fourchette en cupronickel recevra plus de chaleur car la chaleur spécifique du cupronickel est supérieure à celle de l'argent.
733. Un morceau de plomb et un morceau de fonte de même masse ont été frappés trois fois avec une masse. Quelle pièce est devenue la plus chaude ?
Le plomb deviendra plus chaud car sa capacité thermique spécifique est inférieure à celle de la fonte et il faut moins d’énergie pour chauffer le plomb.
734. Un flacon contient de l'eau, l'autre contient du kérosène de même masse et température. Un cube de fer également chauffé a été déposé dans chaque flacon. Qu'est-ce qui va chauffer davantage haute température– de l'eau ou du kérosène ?
Kérosène.
735. Pourquoi les fluctuations de température en hiver et en été sont-elles moins fortes dans les villes situées en bord de mer que dans les villes situées à l'intérieur des terres ?
L'eau se réchauffe et se refroidit plus lentement que l'air. En hiver, il se rafraîchit et bouge messes chaudes l'air sur terre, rendant le climat de la côte plus chaud.
736. La capacité thermique spécifique de l’aluminium est de 920 J/kg °C. Qu'est-ce que cela signifie?
Cela signifie que pour chauffer 1 kg d’aluminium de 1 °C, il faut dépenser 920 J.
737. Les barres d'aluminium et de cuivre de même masse 1 kg sont refroidies à 1 °C. Dans quelle mesure l’énergie interne de chaque bloc va-t-elle changer ? Pour quelle barre cela changera-t-il le plus et de combien ?
738. Quelle quantité de chaleur est nécessaire pour chauffer un kilogramme de billette de fer à 45 °C ?

739. Quelle quantité de chaleur est nécessaire pour chauffer 0,25 kg d'eau de 30 °C à 50 °C ?
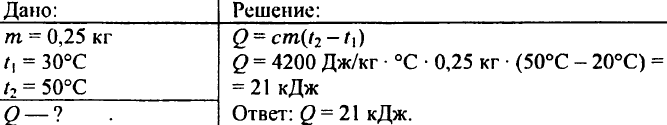
740. Comment l'énergie interne de deux litres d'eau changera-t-elle lorsqu'elle sera chauffée à 5 °C ?

741. Quelle quantité de chaleur faut-il pour chauffer 5 g d'eau de 20 °C à 30 °C ?

742. Quelle quantité de chaleur est nécessaire pour chauffer une boule d'aluminium pesant 0,03 kg à 72 °C ?

743. Calculez la quantité de chaleur nécessaire pour chauffer 15 kg de cuivre à 80 °C.

744. Calculez la quantité de chaleur nécessaire pour chauffer 5 kg de cuivre de 10 °C à 200 °C.

745. Quelle quantité de chaleur est nécessaire pour chauffer 0,2 kg d'eau de 15 °C à 20 °C ?

746. L'eau pesant 0,3 kg s'est refroidie de 20 °C. Dans quelle mesure l’énergie interne de l’eau a-t-elle diminué ?

747. Quelle quantité de chaleur est nécessaire pour chauffer 0,4 kg d'eau à une température de 20 °C jusqu'à une température de 30 °C ?

748. Quelle quantité de chaleur est dépensée pour chauffer 2,5 kg d'eau à 20 °C ?

749. Quelle quantité de chaleur a été dégagée lorsque 250 g d'eau ont refroidi de 90 °C à 40 °C ?

750. Quelle quantité de chaleur est nécessaire pour chauffer 0,015 litre d’eau de 1 °C ?

751. Calculer la quantité de chaleur nécessaire pour chauffer un étang d'un volume de 300 m3 à 10 °C ?

752. Quelle quantité de chaleur faut-il ajouter à 1 kg d'eau pour augmenter sa température de 30 °C à 40 °C ?

753. L'eau d'un volume de 10 litres est passée d'une température de 100 °C à une température de 40 °C. Quelle quantité de chaleur a été dégagée pendant cela ?

754. Calculez la quantité de chaleur nécessaire pour chauffer 1 m3 de sable à 60 °C.

755. Volume d'air 60 m3, capacité thermique spécifique 1000 J/kg °C, densité de l'air 1,29 kg/m3. Quelle quantité de chaleur faut-il pour la porter à 22°C ?

756. L'eau a été chauffée à 10 °C, dépensant 4,20 103 J de chaleur. Déterminez la quantité d’eau.

757. 20,95 kJ de chaleur ont été transmis à de l'eau pesant 0,5 kg. Quelle est la température de l’eau si la température initiale de l’eau était de 20 °C ?

758. Une casserole en cuivre pesant 2,5 kg est remplie de 8 kg d'eau à 10 °C. Quelle quantité de chaleur faut-il pour faire bouillir l’eau de la casserole ?

759. Un litre d'eau à une température de 15 °C est versé dans une louche en cuivre pesant 300 g. Quelle quantité de chaleur est nécessaire pour chauffer l'eau de la louche à 85 °C ?

760. Un morceau de granit chauffé pesant 3 kg est placé dans l'eau. Le granit transfère 12,6 kJ de chaleur à l’eau, refroidissant de 10 °C. Quelle est la capacité thermique spécifique de la pierre ?

761. De l'eau chaude à 50 °C a été ajoutée à 5 kg d'eau à 12 °C, obtenant un mélange à une température de 30 °C. Combien d'eau as-tu ajouté ?

762. De l'eau à 20 °C a été ajoutée à 3 litres d'eau à 60 °C, obtenant ainsi de l'eau à 40 °C. Combien d'eau as-tu ajouté ?

763. Quelle sera la température du mélange si l'on mélange 600 g d'eau à 80 °C avec 200 g d'eau à 20 °C ?

764. Un litre d'eau à 90 °C a été versé dans de l'eau à 10 °C et la température de l'eau est devenue 60 °C. Combien étaient eau froide?

765. Déterminer la quantité à verser dans le récipient eau chaude, chauffé à 60 °C, si le récipient contient déjà 20 litres d'eau froide à une température de 15 °C ; la température du mélange doit être de 40 °C.

766. Déterminez la quantité de chaleur nécessaire pour chauffer 425 g d'eau à 20 °C.

767. De combien de degrés 5 kg d'eau chaufferont-ils si l'eau reçoit 167,2 kJ ?

768. Quelle quantité de chaleur est nécessaire pour chauffer m grammes d'eau à la température t1 jusqu'à la température t2 ?
769. 2 kg d'eau sont versés dans un calorimètre à une température de 15 °C. À quelle température l’eau du calorimètre chauffera-t-elle si on y descend un poids en laiton de 500 g chauffé à 100 °C ? La capacité thermique spécifique du laiton est de 0,37 kJ/(kg °C).

770. Il existe des morceaux de cuivre, d'étain et d'aluminium de même volume. Laquelle de ces pièces a la plus grande et laquelle a la plus petite capacité thermique ?

771. 450 g d'eau ont été versés dans le calorimètre dont la température était de 20 °C. Lorsque 200 g de limaille de fer chauffée à 100 °C étaient immergés dans cette eau, la température de l'eau atteignait 24 °C. Déterminez la capacité thermique spécifique de la sciure de bois.

772. Un calorimètre en cuivre pesant 100 g contient 738 g d'eau dont la température est de 15 °C. 200 g de cuivre ont été plongés dans ce calorimètre à une température de 100 °C, après quoi la température du calorimètre s'est élevée à 17 °C. Quelle est la capacité thermique spécifique du cuivre ?
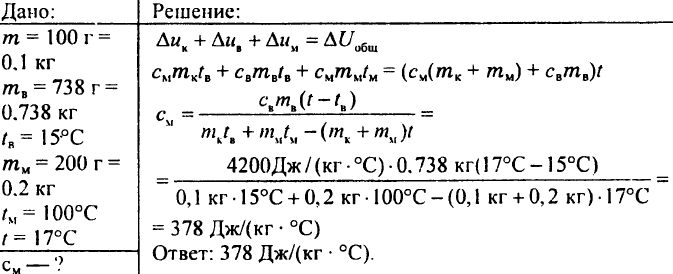
773. Une bille d'acier pesant 10 g est sortie du four et placée dans l'eau à une température de 10 °C. La température de l'eau est montée à 25 °C. Quelle était la température de la boule dans le four si la masse d'eau était de 50 g ? La capacité thermique spécifique de l'acier est de 0,5 kJ/(kg °C).

777. 50 g d'eau à 19 °C ont été versés dans de l'eau pesant 150 g à une température de 35 °C. Quelle est la température du mélange ?

778. De l'eau pesant 5 kg à 90 °C a été versée dans une marmite en fonte pesant 2 kg à une température de 10 °C. Quelle était la température de l'eau ?

779. Un couteau en acier pesant 2 kg a été chauffé à une température de 800 °C puis descendu dans un récipient contenant 15 litres d'eau à une température de 10 °C. Jusqu’à quelle température l’eau du récipient sera-t-elle chauffée ?

(Indication : Pour résoudre ce problème, il est nécessaire de créer une équation dans laquelle la température inconnue est considérée comme la température inconnue de l'eau dans le récipient après l'abaissement du couteau.)
780. Quelle température atteindra l'eau si vous mélangez 0,02 kg d'eau à 15 °C, 0,03 kg d'eau à 25 °C et 0,01 kg d'eau à 60 °C ?

781. Pour chauffer une classe bien ventilée, la quantité de chaleur nécessaire est de 4,19 MJ par heure. L'eau entre dans les radiateurs de chauffage à 80 °C et en sort à 72 °C. Quelle quantité d’eau doit être fournie aux radiateurs chaque heure ?

782. Du plomb pesant 0,1 kg à une température de 100 °C a été immergé dans un calorimètre en aluminium pesant 0,04 kg contenant 0,24 kg d'eau à une température de 15 °C. Après quoi la température dans le calorimètre atteint 16 °C. Quelle est la chaleur spécifique du plomb ?

ÉCHANGE DE CHALEUR.
1. Transfert de chaleur.
Échange de chaleur ou transfert de chaleur est le processus de transfert de l’énergie interne d’un corps à un autre sans effectuer de travail.
Il existe trois types de transfert de chaleur.
1) Conductivité thermique- Il s'agit d'un échange thermique entre les corps lors de leur contact direct.
2) Convection- Il s'agit d'un échange de chaleur dans lequel la chaleur est transférée par des flux de gaz ou de liquide.
3) Radiation– Il s’agit d’un échange de chaleur par rayonnement électromagnétique.
2. Quantité de chaleur.
La quantité de chaleur est une mesure de la variation de l’énergie interne d’un corps lors d’un échange thermique. Désigné par la lettre Q.
Unité de mesure de la quantité de chaleur = 1 J.
La quantité de chaleur reçue par un corps d'un autre corps à la suite d'un échange de chaleur peut être dépensée pour augmenter la température (augmentation de l'énergie cinétique des molécules) ou modifier l'état d'agrégation (augmentation de l'énergie potentielle).
3. Capacité thermique spécifique de la substance.
L'expérience montre que la quantité de chaleur nécessaire pour chauffer un corps de masse m de la température T 1 à la température T 2 est proportionnelle à la masse du corps m et à la différence de température (T 2 - T 1), c'est-à-dire
Q = cm(T. 2 -T 1 ) = smΔ T,
Avec est appelée la capacité thermique spécifique de la substance du corps chauffé.
![]()
La capacité thermique spécifique d'une substance est égale à la quantité de chaleur qui doit être transmise à 1 kg de substance pour la chauffer de 1 K.
Unité de mesure de la capacité thermique spécifique =.
Les valeurs de capacité thermique de diverses substances peuvent être trouvées dans des tableaux physiques.
Exactement la même quantité de chaleur Q sera libérée lorsque le corps sera refroidi de ΔT.
4. Chaleur spécifique de vaporisation.
L'expérience montre que la quantité de chaleur nécessaire pour transformer un liquide en vapeur est proportionnelle à la masse du liquide, c'est-à-dire
Q = Lm,
où est le coefficient de proportionnalité L appelé chaleur spécifique vaporisation.
La chaleur spécifique de vaporisation est égale à la quantité de chaleur nécessaire pour transformer 1 kg de liquide à ébullition en vapeur.
Une unité de mesure pour la chaleur spécifique de vaporisation.
Au cours du processus inverse, la condensation de la vapeur, la chaleur est libérée dans la même quantité que celle dépensée pour la formation de vapeur.
5. Chaleur spécifique de fusion.
L'expérience montre que la quantité de chaleur nécessaire à la transformation solide en liquide, proportionnellement au poids corporel, c'est-à-dire
Q = λ m,
où le coefficient de proportionnalité λ est appelé chaleur spécifique de fusion.
La chaleur spécifique de fusion est égale à la quantité de chaleur nécessaire pour transformer un corps solide pesant 1 kg en liquide au point de fusion.
Unité de mesure de la chaleur spécifique de fusion.
Au cours du processus inverse, la cristallisation du liquide, la chaleur est libérée dans la même quantité que celle dépensée pour la fusion.
6. Chaleur spécifique de combustion.
L'expérience montre que la quantité de chaleur dégagée lors de la combustion complète du carburant est proportionnelle à la masse du carburant, c'est-à-dire
Q = qm,
Où le coefficient de proportionnalité q est appelé chaleur spécifique de combustion.
La chaleur spécifique de combustion est égale à la quantité de chaleur dégagée lors de la combustion complète de 1 kg de carburant.
Unité de mesure de la chaleur spécifique de combustion.
7. Équation du bilan thermique.
L'échange de chaleur implique deux corps ou plus. Certains corps dégagent de la chaleur tandis que d’autres en reçoivent. L'échange de chaleur se produit jusqu'à ce que les températures des corps deviennent égales. Selon la loi de conservation de l’énergie, la quantité de chaleur émise est égale à la quantité reçue. Sur cette base, l'équation du bilan thermique est écrite.
Regardons un exemple.
Un corps de masse m 1, dont la capacité thermique est c 1, a une température T 1, et un corps de masse m 2, dont la capacité thermique est c 2, a une température T 2. De plus, T 1 est supérieur à T 2. Ces corps sont mis en contact. L'expérience montre qu'un corps froid (m 2) commence à se réchauffer et qu'un corps chaud (m 1) commence à se refroidir. Cela suggère qu'une partie de l'énergie interne du corps chaud est transférée au corps froid et que les températures sont égalisées. Notons la température globale finale par θ. 
La quantité de chaleur transférée d'un corps chaud à un corps froid
Q transféré. = c 1 m 1 (T. 1 – θ )
La quantité de chaleur reçue par un corps froid d'un corps chaud
Q reçu. = c 2 m 2 (θ – T 2 )
Selon la loi de conservation de l'énergie Q transféré. = Q reçu., c'est à dire.
c 1 m 1 (T. 1 – θ )= c 2 m 2 (θ – T 2 )
Ouvrons les parenthèses et exprimons la valeur de la température totale en régime permanent θ.
![]()
Dans ce cas, nous obtenons la valeur de température θ en kelvins.
Cependant, puisque Q est passé dans les expressions. et Q est reçu. est la différence entre deux températures, et elle est la même en Kelvin et en degrés Celsius, alors le calcul peut être effectué en degrés Celsius. Alors
![]()
Dans ce cas, nous obtenons la valeur de température θ en degrés Celsius.
L'égalisation des températures résultant de la conductivité thermique peut être expliquée sur la base de la théorie de la cinétique moléculaire comme l'échange d'énergie cinétique entre molécules lors d'une collision au cours d'un mouvement thermique chaotique.
Cet exemple peut être illustré par un graphique. 
Dans cette leçon, nous apprendrons à calculer la quantité de chaleur nécessaire pour chauffer un corps ou libérée par celui-ci lors du refroidissement. Pour ce faire, nous résumerons les connaissances acquises lors des leçons précédentes.
De plus, nous apprendrons, à l'aide de la formule de la quantité de chaleur, à exprimer les quantités restantes à partir de cette formule et à les calculer, connaissant d'autres quantités. Un exemple de problème avec une solution pour calculer la quantité de chaleur sera également considéré.
Cette leçon est consacrée au calcul de la quantité de chaleur lorsqu'un corps est chauffé ou libérée lorsqu'il est refroidi.
La capacité de calculer la quantité de chaleur requise est très importante. Cela peut être nécessaire, par exemple, pour calculer la quantité de chaleur qui doit être transmise à l'eau pour chauffer une pièce.
Riz. 1. La quantité de chaleur qui doit être transmise à l'eau pour chauffer la pièce
Ou pour calculer la quantité de chaleur dégagée lorsque le carburant est brûlé dans divers moteurs :

Riz. 2. La quantité de chaleur dégagée lorsque le carburant brûle dans le moteur
Ces connaissances sont également nécessaires, par exemple, pour déterminer la quantité de chaleur dégagée par le Soleil et tombant sur la Terre :

Riz. 3. La quantité de chaleur dégagée par le Soleil et tombant sur la Terre
Pour calculer la quantité de chaleur, vous devez savoir trois choses (Fig. 4) :
- le poids corporel (qui peut généralement être mesuré à l’aide d’une balance) ;
- la différence de température par laquelle un corps doit être chauffé ou refroidi (généralement mesurée à l'aide d'un thermomètre) ;
- capacité thermique spécifique du corps (qui peut être déterminée à partir du tableau).

Riz. 4. Ce que vous devez savoir pour déterminer
La formule par laquelle la quantité de chaleur est calculée ressemble à ceci :
Les quantités suivantes apparaissent dans cette formule :
La quantité de chaleur mesurée en joules (J);
La capacité thermique spécifique d'une substance se mesure en ;
- différence de température, mesurée en degrés Celsius ().
Considérons le problème du calcul de la quantité de chaleur.
Tâche
Un verre en cuivre d'une masse de grammes contient de l'eau d'un volume de litre à une température. Quelle quantité de chaleur faut-il transférer à un verre d'eau pour que sa température devienne égale à ?

Riz. 5. Illustration des conditions problématiques
Nous écrivons d’abord une courte condition ( Donné) et convertissez toutes les quantités dans le système international (SI).
|
Donné: |
SI |
|
|
Trouver: |
Solution:
Tout d’abord, déterminez de quelles autres quantités nous avons besoin pour résoudre ce problème. En utilisant le tableau de capacité thermique spécifique (Tableau 1), nous trouvons (capacité thermique spécifique du cuivre, puisque par condition le verre est du cuivre), (capacité thermique spécifique de l'eau, puisque par condition il y a de l'eau dans le verre). De plus, nous savons que pour calculer la quantité de chaleur, nous avons besoin d’une masse d’eau. Selon la condition, on nous donne uniquement le volume. Par conséquent, à partir du tableau, nous prenons la densité de l'eau : (Tableau 2).
Tableau 1. Capacité thermique spécifique de certaines substances,
Tableau 2. Densités de certains liquides
Nous avons désormais tout ce dont nous avons besoin pour résoudre ce problème.
Notez que la quantité de chaleur finale sera constituée de la somme de la quantité de chaleur nécessaire pour chauffer le verre en cuivre et de la quantité de chaleur nécessaire pour chauffer l'eau qu'il contient :
Calculons d'abord la quantité de chaleur nécessaire pour chauffer un verre en cuivre :
Avant de calculer la quantité de chaleur nécessaire pour chauffer l'eau, calculons la masse d'eau à l'aide d'une formule qui nous est familière dès la 7e année :
On peut maintenant calculer :
On peut alors calculer :
Rappelons ce que signifient les kilojoules. Le préfixe « kilo » signifie ![]() .
.
Répondre:.
Pour faciliter la résolution des problèmes de recherche de la quantité de chaleur (les problèmes dits directs) et des quantités associées à ce concept, vous pouvez utiliser le tableau suivant.
|
Quantité requise |
Désignation |
Unités |
Formule de base |
Formule pour la quantité |
|
Quantité de chaleur |
