Alkeny jsou třídou organických sloučenin, které mají dvojnou vazbu mezi atomy uhlíku, strukturní vzorec-CnH2n. Dvojná vazba v molekulách olefinu je jedna σ-vazba a jedna π-vazba. Pokud si tedy představíme dva atomy uhlíku a položíme je do roviny, vazba σ bude umístěna v rovině a vazba π bude umístěna nad a pod rovinou (pokud netušíte, o čem mluvíme, viz. část o chemických vazbách).
Hybridizace
V alkenech probíhá hybridizace sp 2, pro kterou úhel H-C-H je 120 stupňů a délka vazby C=C je 0,134 nm.
Struktura
Z přítomnosti vazby π vyplývá a je experimentálně potvrzeno, že:
- Dvojná vazba v molekulách alkenů je podle své struktury citlivější na vnější vlivy než obvyklá vazba σ
- Dvojná vazba znemožňuje rotaci kolem vazby σ, což implikuje přítomnost izomerů, tyto izomery se nazývají cis- a trans-
- Vazba π je méně silná než vazba σ, protože elektrony jsou dále od středů atomů
Fyzikální vlastnosti
Fyzikální vlastnosti alkenů jsou podobné fyzikálním vlastnostem alkanů. Alkeny, které mají až pět atomů uhlíku, jsou v plynném stavu at normální podmínky. Molekuly obsahující od šesti do 16 atomů uhlíku jsou za normálních podmínek v kapalném stavu a od 17 atomů uhlíku - alkeny jsou v pevném stavu.
Bod varu alkenů se zvyšuje v průměru o 30 stupňů pro každou skupinu CH 2, stejně jako alkany, větve snižují bod varu látky.
Přítomnost vazby π způsobuje, že olefiny jsou mírně rozpustné ve vodě, což způsobuje jejich nízkou polaritu. Alkeny jsou nepolární látky a rozpouštějí se v nepolárních rozpouštědlech a slabě polárních rozpouštědlech.
Hustota alkenů je vyšší než hustota alkanů, ale nižší než hustota vody
izomerismus
- Izomerie uhlíkového skeletu: 1-buten a 2-methylpropen
- Izomerie polohy dvojné vazby: 1-buten a 2-buten
- Mezitřídní izomerie: 1-buten a cyklobutan
Reakce
Charakteristické reakce alkenů jsou adiční reakce, vazba π se přeruší a vzniklé elektrony ochotně přijímají nový prvek. Přítomnost π vazby znamená větší množství energie, proto jsou adiční reakce zpravidla exotermické povahy, tzn. pokračujte s uvolňováním tepla.
Adiční reakce
Přídavek halogenovodíků
Halogenidy vodíku se snadno přidávají na dvojnou vazbu alkenů a vytvářejí halogenidy l s. Halogenidy se mísí s kyselinou octovou nebo přímo, v plynném stavu, s alkenem. Chcete-li zvážit mechanismus reakce, musíte znát Markovnikovovo pravidlo.
Markovnikovovo pravidlo
Když homology ethylenu interagují s kyselinami, vodík se váže k více hydrogenovanému atomu uhlíku.
Výjimka z pravidla, hydroborace alkynů, bude diskutována v článku o alkynech.
Reakční mechanismus adice halogenovodíků na alkeny je následující: dochází k homolytickému štěpení vazby v molekule halogenovodíku, vzniká proton a halogenový anion. Proton se přidává k alkenu za vzniku karbokationtu, tato reakce je endotermická a má vysoká úroveň aktivační energie, takže reakce probíhá pomalu. Vytvořený karbokation je velmi reaktivní, takže se snadno váže na halogen, aktivační energie je nízká, takže tento krok neinhibuje reakci.
Při pokojové teplotě reagují alkeny s chlorem a bromem v přítomnosti tetrachlormethanu. Mechanismus adiční reakce halogenu je následující: elektrony z vazby π působí na molekulu halogenu X 2 . Jakmile se halogen přiblíží k olefinu, elektrony v molekule halogenu se posunou ke vzdálenějšímu atomu, molekula halogenu se tak polarizuje, nejbližší atom má kladný náboj, vzdálenější záporný náboj. Dochází k heterolytickému štěpení vazby v molekule halogenu za vzniku kationtu a aniontu. Halogenový kation se váže na dva atomy uhlíku prostřednictvím elektronového páru vazby π a volného elektronového páru kationtu. Zbývající halogenový anion působí na jeden z atomů uhlíku v molekule halogenalkenu a láme se cyklus C-C-X a vytvoření dihalogenalkenu.
Alkenové adiční reakce mají dvě hlavní aplikace, první je kvantitativní analýza, určující počet dvojných vazeb počtem absorbovaných molekul X2. Druhý je v průmyslu. Výroba plastů je založena na vinylchloridu. Trichlorethylen a tetrachlorethylen jsou vynikajícími rozpouštědly pro acetylenové tuky a kaučuky.
Hydrogenace
Přidání plynného vodíku k alkenu nastává s Pt, Pd nebo Ni katalyzátory. V důsledku reakce vznikají alkany. Hlavní aplikací katalytické adiční reakce vodíku je za prvé kvantitativní analýza. Na základě zbytku molekul H2 můžete určit počet dvojných vazeb v látce. Za druhé, rostlinné tuky a rybí oleje jsou nenasycené uhlíky a taková hydrogenace vede ke zvýšení bod tání, přeměna na pevné tuky. Na tomto procesu je založena výroba margarínu.
Hydratace
Když se alkeny smíchají s kyselinou sírovou, vytvoří se alkylhydrogensulfáty. Když se alkylhydrogensírany zředí vodou a za současného zahřívání se vytvoří alkohol. Příkladem reakce je smíchání ethenu (ethylenu) s kyselinou sírovou, následné smíchání s vodou a zahřátí, výsledkem je ethanol.
Oxidace
Alkeny se snadno oxidují různými látkami, jako je například KMnO 4, O 3, OsO 4 atd. Existují dva typy oxidace alkenů: štěpení vazby π bez porušení vazby σ a štěpení vazeb σ a π. Oxidace bez porušení sigma vazby se nazývá měkká oxidace, zatímco rozbití sigma vazby se nazývá tvrdá oxidace.
Oxidací ethenu bez porušení vazby σ vznikají epoxidy (epoxidy jsou cyklické C-C-O sloučeniny) nebo dvojsytné alkoholy. Oxidací se štěpením vazby σ vznikají acetony, aldehydy a karboxylové kyseliny.
Oxidace manganistanem draselným
Oxidační reakce alkenů pod vlivem manganistanu draselného se nazývají objevené Egorem Vagnerem a nesou jeho jméno. Při Wagnerově reakci dochází k oxidaci v organickém rozpouštědle (aceton nebo ethanol) při teplotě 0-10°C, ve slabém roztoku manganistanu draselného. V důsledku reakce se tvoří dvojsytné alkoholy a dochází ke změně barvy manganistanu draselného.
Polymerizace
Většina jednoduchých alkenů může podléhat samoadičním reakcím, a tak tvořit velké molekuly ze strukturních jednotek. Takové velké molekuly se nazývají polymery; reakce, při které vzniká polymer, se nazývá polymerace. Jednoduché strukturní jednotky, které tvoří polymery, se nazývají monomery. Polymer je označen uzavřením opakující se skupiny v závorkách s indexem "n". velký počet opakování, například: "-(CH2-CH2)n-" - polyethylen. Polymerizační procesy jsou základem pro výrobu plastů a vláken.
Radikálová polymerace
Radikálová polymerace je iniciována pomocí katalyzátoru - kyslíku nebo peroxidu. Reakce se skládá z tři etapy:
Zahájení
ROOR → 2RO.
CH 2 = CH-C6H5 → RO - CH2C. H-C6H5
Růst řetězce
R.O. - CH2C. H-C6H5 + CH2=CH-C6H5 -> RO-CH2-CH(C6H5)-CH2-C. -C5H6
Ukončení řetězce rekombinací
CH2-C. H-C6H5 + CH2-C. H-C6H5 → CH2-CH-C6H5-CH2-CH-C6H5
Přerušení obvodu disproporcí
CH2-C. H-C6H5 + CH2-C. H-C6H5 → CH=CH-C6H5 + CH2-CH2-C6H5
Iontová polymerace
Dalším způsobem polymerace alkenů je iontová polymerace. Reakce probíhá za vzniku meziproduktů - karbokationtů a karbanionů. Tvorba prvního karbokationtu se obvykle provádí za použití Lewisovy kyseliny, tvorba karbaniontu se proto provádí reakcí s Lewisovou bází.
A + CH2=CH-X → A-CH2-C + H-X → ... → A-CH2-CHX-CH2-CHX-CH2C + HX ...
B + CH2=CH-X → B-CH2-C - H-X → ... → B-CH2-CHX-CH2-CHX-CH2C - HX ...
Běžné polymery
Nejběžnější polymery jsou:
Nomenklatura
Název alkenů, podobně jako alkany, se skládá z první části - předpony udávající počet atomů uhlíku v hlavním řetězci a přípony -en. Alken je sloučenina s dvojnou vazbou, takže molekuly alkenu začínají dvěma atomy uhlíku. První na seznamu je ethen, eth- - dva atomy uhlíku, -en - přítomnost dvojné vazby.
Pokud jsou v molekule více než tři atomy uhlíku, musí být uvedena poloha dvojné vazby, například buten může být dvou typů:
CH2=CH-CH2-CH3
CH3-CH=CH-CH3
Pro označení polohy dvojné vazby je potřeba přidat číslo, pro příklad výše by to byl 1-buten, respektive 2-buten (používají se i názvy 1-buten a 2-buten, ale nejsou systematický).
Přítomnost dvojné vazby znamená izomerii, kdy se molekuly mohou nacházet různé strany z dvojné vazby, např.
Tento izomerismus se nazývá cis- (Z-zusammen, z němčiny dohromady) a trans- (E-entgegen, opak němčiny), v prvním případě cis-1,2-dichlorethen (nebo (Z)-1,2-dichlorethen ), ve druhém - trans-1,2-dichlorethen (nebo (E)-1,2-dichlorethen).
Alkeny jsou aktivnější třídou látek než alkany. Chemické vlastnosti alkenů jsou určeny strukturou jejich molekul.
Struktura
Nenasycené uhlovodíky – alkeny nebo olefiny – se od ostatních tříd organických látek liší přítomností dvojné nebo π vazby mezi atomy uhlíku. Dvojná vazba může být umístěna kdekoli v molekule.
Pí vazba je tvořena překrývajícími se p orbitaly. Vzhledem k tomu, že p-orbital má prodloužení v obou směrech od osy a připomíná činku, vyskytuje se pí-vazba na dvou místech. Na rozdíl od vazby σ, ke které dochází, když se orbitaly s překrývají ve formě koule, je vazba π méně pevná a snadno se ničí jinými sloučeninami. To určuje aktivitu alkenů.

Rýže. 1. π-vazba a σ-vazba.
Dvojná vazba působí při adičních reakcích jako donor elektronů. Proto jsou alkeny charakterizovány elektrofilními adičními reakcemi.
Fyzikální vlastnosti
Jsou běžné fyzikální vlastnosti alkeny:
- teploty tání a varu se zvyšují se zvyšující se molekulovou hmotností v homologní řadě;
- nerozpouštějí se ve vodě;
- držet na vodní hladině, protože mají hustotu mnohonásobně větší menší hustota voda;
- rozpouštět v organických rozpouštědlech - alkoholy, ethery.
Stav agregace látek se mění v závislosti na počtu atomů uhlíku v homologní řadě. Alkeny s 2-4 atomy uhlíku jsou plyny. Od peptenu (C 5 H 10) po heptadecen (C 17 H3 4) jsou látky v kapalném stavu. Alkeny obsahující více než 17 atomů uhlíku jsou pevné látky.

Rýže. 2. Homologní série alkeny
Chemické vlastnosti
Vlastnosti a příklady chemických vlastností alkenů jsou uvedeny v tabulce.
|
Reakce |
Popis |
Reakční rovnice |
|
Hydrogenace - přídavek vodíku |
Vyskytuje se v vysoký krevní tlak v přítomnosti katalyzátoru - niklu, palladia nebo platiny. Vznikají alkany – nasycené uhlovodíky |
CH2=CH-CH3 + H2 -> CH3-CH2-CH3 |
|
Halogenace - adice halogenů |
Vyskytuje se v normální podmínky. Halogeny se přidávají přes dvojnou vazbu. Vznikají dihalogenalkany |
CH2=CH2 + Cl2 -> Cl-CH2-CH2-Cl (1,2-dichlorethan); CH3-CH=CH-CH3 + Br2 → CH3-CH-Br-CH-Br-CH3 (2,3-dibrombutan) |
|
Hydrohalogenace - adice halogenovodíků |
Elektrofilní adiční reakce. Elektrofil je vodíkový proton v halogenu. Vznikají halogenalkany |
CH 2 =CH 2 + HCl → CH 3-CH 2-Cl (chlorethan) |
|
Hydratace – přídavek vody |
Reakce probíhá v přítomnosti anorganické kyseliny- sírová, fosforečná. Působí jako katalyzátor a jsou zdrojem vodíku. Vznikají jednosytné alkoholy |
CH2=CH2 + H20 -> CH3-CH20H |
|
Polymerizace - zvýšení počtu atomů |
Vyskytuje se v přítomnosti katalyzátoru při zvýšeném tlaku a teplotě. Tímto způsobem se vyrábí polyethylen, polyvinylchlorid, polypropylen |
nCH2=CH2-» (-CH2-CH2-)n |
|
Vyskytuje se při přebytku kyslíku |
CH2=CH2 + 302 -> 2C02 + H20 |
|
|
Neúplná oxidace |
Vyskytuje se v přítomnosti katalyzátoru. Alken smíchaný s kyslíkem se vede přes zahřáté stříbro. Vzniká epoxid – alkenoxid |
2CH2=CH2+02 -> 2CH2-0-CH2 |
|
Wagnerova reakce |
Oxidace manganistanem draselným v alkalickém nebo neutrálním prostředí. Tvoří se alkoholy |
3CH2=CH2 + 2KMnO4 + 4H20 → 3CH2OH-CH2OH + 2KOH + 2Mn02 |
|
Oxidace vroucím manganistanem draselným v kyselém prostředí |
Vznikají karboxylové kyseliny |
CH3-CH=CH-CH3 + 4[0] -> 2CH3COOH |
Při zahřívání v přítomnosti katalyzátoru podléhají alkeny izomerační reakci. Mění se poloha dvojné vazby nebo struktura uhlíkového skeletu. Například buten-1 (poloha dvojné vazby mezi prvním a druhým atomem) se stane butenem-2 (dvojná vazba je „posunutá“ na druhý atom).

Rýže. 3. Izomerizace alkenů.
co jsme se naučili?
V hodině chemie v 10. třídě jsme se dozvěděli o chemických vlastnostech alkenů. Dvojná vazba činí tyto látky aktivnějšími než alkany. Alkeny interagují s halogeny, kyslíkem, vodou, vodíkem a halogenovodíky. Většina reakcí probíhá v přítomnosti katalyzátoru při vysoké teplotě nebo při vysoký krevní tlak. Alkeny tvoří polymery. Také pod vlivem katalyzátorů se tvoří izomery.
Test na dané téma
Vyhodnocení zprávy
Průměrné hodnocení: 4.6. Celkem obdržených hodnocení: 64.
NENASYCENÉ NEBO NENAsycené Uhlovodíky ETYLENOVÉ ŘADY
(ALKENY NEBO OLEFINY)
alkeny nebo olefiny(z latiny olefiant - olej - starý název, ale široce používaný v chemické literatuře. Důvodem tohoto názvu bylo ethylenchlorid, získaný v 18. století, je kapalná, olejovitá látka.) - alifatické nenasycené uhlovodíky, v jejichž molekulách je mezi atomy uhlíku jedna dvojná vazba.
Alkeny obsahují ve své molekule méně atomů vodíku než jejich odpovídající alkany (se stejným počtem atomů uhlíku), proto se takové uhlovodíky nazývají neomezený nebo nenasycené.
Alkeny tvoří homologickou řadu s obecným vzorcem CnH2n
1. Homologní řada alkenů
|
S n H 2 n alken |
Jména, přípona EH, ILENE |
|
C2H4 |
tento en, tento Ilen |
|
C3H6 |
propen |
|
C4H8 |
buten |
|
C5H10 |
penten |
|
C6H12 |
hexen |
Homology:
SH 2 = CH 2 ethen
SH 2 = CH- CH 3 propen
SH2=CH-CH2-CH3buten-1
SH2=CH-CH2-CH2-CH 3 penten-1
2. Fyzikální vlastnosti
Ethylen (ethene) je bezbarvý plyn s velmi slabým nasládlým zápachem, mírně lehčí než vzduch, mírně rozpustný ve vodě.
C 2 – C 4 (plyny)
C 5 – C 17 (kapaliny)
C 18 – (pevné)
· Alkeny jsou nerozpustné ve vodě, rozpustné v organických rozpouštědlech (benzín, benzen atd.)
Lehčí než voda
S rostoucím Mr se zvyšují body tání a varu
3. Nejjednodušší alken je etylen - C2H4
Strukturní a elektronické vzorce ethylenu jsou:
V molekule ethylenu dochází k hybridizaci s- a dva p-orbitaly atomů C ( sp 2 -hybridizace).
Každý atom C má tedy tři hybridní orbitaly a jeden nehybridní p-orbitaly. Dva z hybridních orbitalů atomů uhlíku se vzájemně překrývají a tvoří mezi atomy uhlíku
σ - vazba. Zbývající čtyři hybridní orbitaly atomů C se překrývají ve stejné rovině se čtyřmi s-orbitaly atomů H a tvoří také čtyři σ - vazby. Dvě nehybridní p-orbitaly atomů C se vzájemně překrývají v rovině, která je umístěna kolmo na rovinu σ-vazby, tzn. jeden se tvoří P- spojení.

Od přírody P- spojení se výrazně liší od σ - spojení; P- vazba je méně pevná v důsledku překrytí elektronových mraků mimo rovinu molekuly. Pod vlivem činidel P- spojení se snadno přeruší.
Molekula ethylenu je symetrická; jádra všech atomů jsou umístěna ve stejné rovině a vazebné úhly jsou blízké 120°; vzdálenost mezi středy atomů C je 0,134 nm.
Pokud jsou atomy spojeny dvojnou vazbou, pak je jejich rotace bez elektronových mraků nemožná P- spojení nebylo otevřeno.
4. Izomerie alkenů
Spolu s strukturní izomerie uhlíkového skeletu Alkeny se vyznačují za prvé jinými typy strukturní izomerie - izomerie vícenásobné pozice vazby A mezitřídní izomerie.
Za druhé, v řadě alkenů se objevuje prostorová izomerie , spojené s různými polohami substituentů vzhledem k dvojné vazbě, kolem kterých je intramolekulární rotace nemožná.
Strukturní izomerie alkenů
1. Izomerie uhlíkového skeletu (počínaje C 4 H 8):
2. Izomerie polohy dvojné vazby (počínaje C 4 H 8):
3. Mezitřídní izomerie s cykloalkany, počínaje C 3 H 6:
Prostorová izomerie alkenů
Rotace atomů kolem dvojné vazby je nemožná bez jejího porušení. To je způsobeno strukturálními rysy p-vazby (mrak p-elektronů je soustředěn nad a pod rovinou molekuly). Vzhledem k rigidní fixaci atomů se neobjevuje rotační izomerie vzhledem k dvojné vazbě. Ale stává se to možným cís-trans- izomerie.
Alkeny, které mají různé substituenty na každém ze dvou atomů uhlíku na dvojné vazbě, mohou existovat ve formě dvou prostorových izomerů, které se liší umístěním substituentů vzhledem k rovině p-vazby. Tedy v molekule butenu-2 CH3-CH=CH-CH3 CH3 skupiny mohou být umístěny buď na jedné straně dvojné vazby v cís-izomer, nebo na opačných stranách v trans-izomer.

POZORNOST!
cis-trans- Izomerie se neprojeví, pokud alespoň jeden z atomů C na dvojné vazbě má 2 stejné substituenty.
Například,
buten-1 CH 2 = CH – CH 2 – CH 3 nemá cís- A trans-izomery, protože 1. atom C je vázán na dva stejné atomy H.
Izomery cís- A trans- liší se nejen fyzicky
 ,
,
ale i chemické vlastnosti, protože přiblížení částí molekuly blíže nebo dále od sebe v prostoru podporuje nebo brání chemické interakci.
Někdy cis-trans-izomerie se ne zcela přesně nazývá geometrická izomerie. Nepřesnost je v tom Všechno prostorové izomery se liší nejen svou geometrií cís- A trans-.
5. Názvosloví
Alkeny jednoduché struktury jsou často pojmenovány nahrazením přípony -ane v alkanech s -ylen: ethan - ethylen, propan-propylen atd.
Podle systematického názvosloví se názvy ethylenových uhlovodíků dělají nahrazením přípony -ane v odpovídajících alkanech příponou -en (alkan - alken, ethan - ethen, propan - propen atd.). Volba hlavního řetězce a pořadí pojmenování jsou stejné jako u alkanů. Řetězec však musí nutně obsahovat dvojnou vazbu. Číslování řetězu začíná od konce, ke kterému je toto spojení umístěno nejblíže. Například:

Nenasycené (alkenové) radikály se nazývají triviálními názvy nebo systematickou nomenklaturou:
(H2C=CH-)vinyl nebo ethenyl
(H2C=CH-CH2) allyl
Alkeny se vyznačují především reakcemi přistoupení přes dvojnou vazbu. V zásadě tyto reakce probíhají iontovým mechanismem. Pi vazba je přerušena a jsou vytvořeny dvě nové sigma vazby. Dovolte mi připomenout, že substituční reakce byly typické pro alkany a probíhaly radikálním mechanismem. Molekuly vodíku se mohou vázat na alkeny; tyto reakce se nazývají hydrogenace, molekuly vody, hydratace, halogenace halogenů, hydrohalogenace halogenovodíků. Ale nejdřív.
Adiční reakce dvojné vazby
Tak, První chemická vlastnost schopnost přidávat halogenovodíky, hydrohalogenace.
Propen a další alkeny reagují s halogenovodíky podle Markovnikovova pravidla.

Atom vodíku se váže na nejvíce hydrogenovaný, nebo přesněji hydrogenovaný atom uhlíku.
Druhýčíslem na našem seznamu vlastností by byla hydratace, přídavek vody.
Reakce probíhá při zahřívání v přítomnosti kyseliny, obvykle sírové nebo fosforečné. K přidávání vody dochází také podle Markovnikovova pravidla, to znamená, že primární alkohol lze získat pouze hydratací ethylenu, zbývající nerozvětvené alkeny poskytují sekundární alkoholy.
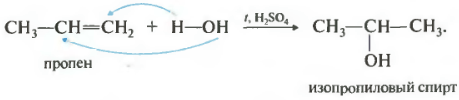
Existují výjimky z Markovnikovova pravidla pro hydrohalogenaci i hydrataci. Za prvé, v rozporu s tímto pravidlem, k přidávání dochází v přítomnosti peroxidů.
Za druhé, pro deriváty alkenů, ve kterých jsou přítomny skupiny přitahující elektrony. Například pro 3,3,3-trifluorpropen-1.

Atomy fluoru díky své vysoké elektronegativitě k sobě přitahují hustotu elektronů podél řetězce sigma vazeb. Tento jev se nazývá negativní indukční efekt.
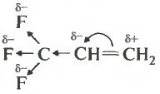
Z tohoto důvodu jsou pohyblivé pí elektrony dvojné vazby přemístěny a nejvzdálenější atom uhlíku skončí s částečným kladným nábojem, který se obvykle označuje jako delta plus. To je to, že záporně nabitý bromový iont půjde a vodíkový kation se připojí k nejméně hydrogenovanému atomu uhlíku.
Kromě trifluormethylové skupiny působí negativně induktivně např. trichlormethylová skupina, nitroskupina, karboxylová skupina a některé další.
Tento druhý případ porušení Markovnikovova pravidla v Jednotné státní zkoušce je velmi vzácný, ale přesto je vhodné na něj pamatovat, pokud plánujete zkoušku složit s maximálním počtem bodů.
Třetí chemická vlastnost připojení molekul halogenu.
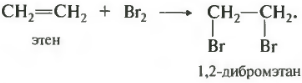
To se týká především bromu, protože tato reakce je kvalitativní pro násobnou vazbu. Když například ethylen prochází bromovou vodou, to znamená roztokem bromu ve vodě, který má hnědou barvu, změní se barva. Když bromovou vodou propustíte směs plynů, například ethanu a ethenu, můžete získat čistý ethan bez příměsí ethenu, protože zůstane v reakční baňce ve formě dibromethanu, což je kapalina.
Zvláště pozoruhodná je reakce alkenů v plynné fázi při silném zahřívání, například s chlórem.
Za takových podmínek neprobíhá adiční reakce, ale substituční reakce. Navíc výhradně na atomu uhlíku alfa, to znamená atomu sousedícího s dvojnou vazbou. V tomto případě se získá 3-chlorpropen-1. Tyto reakce jsou u zkoušky málo časté, takže si je většina studentů nepamatuje a zpravidla chybují.
Čtvrtýčíslo je hydrogenační reakce a s ní i dehydrogenační reakce. Tedy přidání nebo odstranění vodíku.
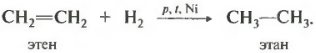
K hydrogenaci dochází při nepříliš vysoké teplotě na niklovém katalyzátoru. Při vyšších teplotách je možná dehydrogenace za vzniku alkynů.
Pátý Vlastností alkenů je schopnost polymerace, kdy stovky a tisíce molekul alkenů tvoří velmi dlouhé a pevné řetězce v důsledku porušení pí vazby a vzniku sigma vazeb mezi sebou.
V tomto případě byl výsledkem polyethylen. Upozorňujeme, že výsledná molekula neobsahuje žádné vícenásobné vazby. Takové látky se nazývají polymery, původní molekuly se nazývají monomery, opakující se fragment je elementární jednotka polymeru a číslo n je stupeň polymerace.
Reakce za vzniku dalších důležitých polymerních materiálů, jako je polypropylen, jsou také možné.


Dalším důležitým polymerem je polyvinylchlorid.
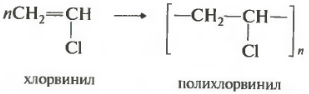
Výchozím materiálem pro výrobu tohoto polymeru je chlorethen, jehož obecný název je vinylchlorid. Protože tento nenasycený substituent se nazývá vinyl. Často se vyskytující zkratka na plastových výrobcích, PVC, znamená polyvinylchlorid.
Diskutovali jsme o pěti vlastnostech, které představovaly adiční reakce dvojné vazby. Nyní se podívejme na reakce oxidace.
Oxidační reakce alkenů
Šestý chemickou vlastností v našem obecném seznamu je mírná oxidace nebo Wagnerova reakce. Vyskytuje se, když je alken vystaven působení vodného roztoku manganistanu draselného za studena, proto se ve zkušebních úlohách často uvádí teplota nula stupňů.
Výsledkem je dvojsytný alkohol. V tomto případě se ethylenglykol a obecně takové alkoholy souhrnně nazývají glykoly. Během reakce se purpurově růžový roztok manganistanu odbarví, takže tato reakce je také kvalitativní pro dvojnou vazbu. Mangan v neutrálním prostředí je redukován z oxidačního stupně +7 na oxidační stupeň +4. Podívejme se na několik dalších příkladů. ROVNICE
Zde získáme propandiol-1,2. Cyklické alkeny však budou reagovat stejným způsobem. ROVNICE
Další možností je, když se dvojná vazba nachází např. v postranním řetězci aromatické uhlovodíky. Pravidelně v zkouškové úkoly Existuje Wagnerova reakce zahrnující styren, jeho druhé jméno je vinylbenzen.

Doufám, že jsem vám poskytl dostatek příkladů, abyste pochopili, že mírná oxidace dvojné vazby se vždy zcela podřídí jednoduché pravidlo Vazba pí se přeruší a ke každému atomu uhlíku se přidá hydroxyskupina.
Nyní k tvrdé oxidaci. Bude to naše sedmý vlastnictví. K této oxidaci dochází, když alken při zahřívání reaguje s kyselým roztokem manganistanu draselného.
Dochází k destrukci molekuly, tedy k její destrukci na dvojné vazbě. V případě butenu-2 byly získány dvě molekuly kyseliny octové. Obecně lze polohu násobné vazby v uhlíkovém řetězci posoudit z oxidačních produktů.
Oxidací 1-butenu vzniká molekula kyseliny propionové (propanové) a oxidu uhličitého.
V případě ethylenu získáte dvě molekuly oxidu uhličitého. Ve všech případech dochází v kyselém prostředí k redukci manganu z oxidačního stavu +7 na +2.
A nakonec osmý vlastnost úplná oxidace nebo spalování.
Alkeny hoří, stejně jako ostatní uhlovodíky, na oxid uhličitý a vodu. Napišme rovnici pro spalování alkenů v obecném tvaru.
V molekule alkenu bude tolik molekul oxidu uhličitého, kolik je atomů uhlíku, protože molekula CO 2 obsahuje jeden atom uhlíku. Tedy n molekul CO 2 . Bude dvakrát méně molekul vody než atomů vodíku, tedy 2n/2, což znamená právě n.
Nalevo i napravo je stejný počet atomů kyslíku. Vpravo jsou 2n oxidu uhličitého plus n vody, celkem 3n. Vlevo je stejný počet atomů kyslíku, což znamená, že molekul je dvakrát méně, protože molekula obsahuje dva atomy. Tedy 3n/2 molekul kyslíku. Můžete napsat 1,5n.
Zkontrolovali jsme osm chemické vlastnosti alkenů.
Alkeny jsou chemicky aktivní. Jejich Chemické vlastnosti jsou do značné míry určeny přítomností dvojné vazby. Nejběžnější reakce pro alkeny jsou elektrofilní adiční reakce a radikálové adiční reakce. Nukleofilní adiční reakce obvykle vyžadují přítomnost silného nukleofilu a nejsou typické pro alkeny. Alkeny snadno podléhají oxidačním a adičním reakcím a jsou také schopné substituce alkylových radikálů.
Adiční reakce
Hydrogenace Přidávání vodíku (hydrogenační reakce) k alkenům se provádí v přítomnosti katalyzátorů. Nejčastěji se používají drcené kovy - platina, nikl, palladium atd. V důsledku toho vznikají odpovídající alkany (nasycené uhlovodíky).
$CH_2=CH_2 + H2 → CH_3–CH_3$
Přídavek halogenů. Alkeny za běžných podmínek snadno reagují s chlorem a bromem za vzniku odpovídajících dihalogenalkanů, ve kterých jsou atomy halogenu umístěny na sousedních atomech uhlíku.
Poznámka 1
Když alkeny interagují s bromem, brom se zbarví na žlutohnědou barvu. Toto je jedno z nejstarších a nejjednodušších kvalitativní reakce na nenasycené uhlovodíky, protože alkyny a alkadieny také reagují podobně.
$CH_2=CH_2 + Br_2 → CH_2Br–CH_2Br$
Přídavek halogenovodíků. Při interakci ethylenových uhlovodíků s halogenovodíky ($HCl$, $HBr$) vznikají halogenalkany, směr reakce závisí na struktuře alkenů.
V případě ethylenu nebo symetrických alkenů probíhá adiční reakce jednoznačně a vede ke vzniku pouze jednoho produktu:
$CH_2=CH_2 + HBr → CH_3–CH_2Br$
V případě nesymetrických alkenů je možná tvorba dvou různých adičních reakčních produktů:
Poznámka 2
Ve skutečnosti vzniká převážně pouze jeden reakční produkt. Vzor ve směru takových reakcí stanovil ruský chemik V.V. Markovnikov v roce 1869 Říká se tomu Markovnikovovo pravidlo. Když halogenovodíky reagují s nesymetrickými alkeny, přidá se atom vodíku v místě štěpení dvojné vazby na nejvíce hydrogenovaném atomu uhlíku, tedy dříve, než se spojí s velkým počtem atomů vodíku.
Markovnikov toto pravidlo formuloval na základě experimentálních dat a teprve mnohem později získalo teoretické zdůvodnění. Uvažujme reakci propylenu s chlorovodíkem.
Jedním z rysů dluhopisu $p$ je jeho schopnost snadné polarizace. Vlivem methylové skupiny (pozitivní indukční efekt + $I$) v molekule propenu se elektronová hustota vazby $p$ posune k jednomu z atomů uhlíku (= $CH_2$). V důsledku toho se na něm objeví částečný záporný náboj ($\delta -$). Na druhém atomu uhlíku dvojné vazby se objeví částečný kladný náboj ($\delta +$).
Toto rozložení elektronové hustoty v molekule propylenu určuje místo budoucího protonového útoku. Toto je atom uhlíku methylenové skupiny (= $CH_2$), který nese částečný záporný $\delta-$ náboj. A chlor podle toho napadá atom uhlíku s částečným kladným nábojem $\delta+$.
V důsledku toho je hlavním produktem reakce propylenu s chlorovodíkem 2-chlorpropan.
Hydratace
Hydratace alkenů probíhá za přítomnosti minerálních kyselin a řídí se Markovnikovovým pravidlem. Produkty reakce jsou alkoholy
$CH_2=CH_2 + H_2O → CH_3–CH_2–OH$
Alkylace
Přidání alkanů k alkenům v přítomnosti kyselého katalyzátoru ($HF$ nebo $H_2SO_4$) při nízké teploty vede ke vzniku uhlovodíků s vyšší molekulovou hmotností a často se používá v průmyslu k výrobě motorových paliv
$R–CH_2=CH_2 + R’–H → R–CH_2–CH_2–R’$
Oxidační reakce
K oxidaci alkenů může docházet v závislosti na podmínkách a typech oxidačních činidel jak při štěpení dvojné vazby, tak při zachování uhlíkového skeletu:
Polymerační reakce
Molekuly alkenů jsou schopny se za určitých podmínek vzájemně adovat s otevřením $\pi$ vazeb a vznikem dimerů, trimerů nebo vysokomolekulárních sloučenin - polymerů. Polymerace alkenů může probíhat buď volným radikálem nebo mechanismem kation-aniont. Jako iniciátory polymerace se používají kyseliny, peroxidy, kovy atd. Polymerační reakce probíhá také pod vlivem teploty, ozáření a tlaku. Typický příklad je polymerace ethylenu za vzniku polyethylenu
$nCH_2=CH_2 → (–CH_2–CH_(2^–))_n$
Substituční reakce
Substituční reakce nejsou pro alkeny typické. Nicméně, když vysoké teploty(nad 400 °C) jsou potlačeny radikálové adiční reakce, které jsou reverzibilní. V tomto případě je možné nahradit atom vodíku umístěný v allylové poloze při zachování dvojné vazby
$CH_2=CH–CH_3 + Cl_2 – CH_2=CH–CH_2Cl + HCl$
