Tepelná kapacita- to je množství tepla absorbovaného tělem při zahřátí o 1 stupeň.
Tepelná kapacita tělesa je označena velkým písmenem Latinské písmeno S.
Na čem závisí tepelná kapacita tělesa? Především z její hmoty. Je jasné, že ohřátí např. 1 kilogramu vody bude vyžadovat více tepla než ohřátí 200 gramů.
A co druh látky? Udělejme experiment. Vezmeme dvě stejné nádoby a nalijeme vodu o hmotnosti 400 g do jedné z nich a do druhé - rostlinný olej o hmotnosti 400 g, začněme je ohřívat pomocí stejných hořáků. Pozorováním údajů teploměru uvidíme, že se olej rychle zahřeje. Aby se voda a olej ohřály na stejnou teplotu, musí se voda ohřívat déle. Čím déle ale vodu ohříváme, tím více tepla dostává od hořáku.
Je tedy potřeba zahřát stejnou hmotu různých látek na stejnou teplotu různá množství teplo. Množství tepla potřebné k zahřátí tělesa a tedy i jeho tepelná kapacita závisí na druhu látky, ze které se těleso skládá.
Takže například ke zvýšení teploty vody o hmotnosti 1 kg o 1 °C je potřeba množství tepla rovné 4200 J a k zahřátí stejné hmoty o 1 °C slunečnicový olej potřebné množství tepla je 1700 J.
Fyzické množství Ukazuje, kolik tepla je potřeba k zahřátí 1 kg látky o 1 ºС specifická tepelná kapacita této látky.
Každá látka má svou specifickou tepelnou kapacitu, která se označuje latinským písmenem c a měří se v joulech na kilogram stupně (J/(kg °C)).
Specifické teplo stejná látka v různých stavech agregace (pevné, kapalné a plynné) je různá. Například měrná tepelná kapacita vody je 4200 J/(kg °C) a měrná tepelná kapacita ledu je 2100 J/(kg °C); hliník v pevném stavu má měrnou tepelnou kapacitu 920 J/(kg - °C), v kapalném stavu - 1080 J/(kg - °C).
Všimněte si, že voda má velmi vysokou specifickou tepelnou kapacitu. Proto voda v mořích a oceánech, která se v létě zahřívá, absorbuje ze vzduchu velký počet teplo. Díky tomu v místech, která se nacházejí v blízkosti velkých vodních ploch, není léto tak horké jako v místech daleko od vody.
Výpočet množství tepla potřebného k zahřátí tělesa nebo jím uvolněného při ochlazování.
Z výše uvedeného je zřejmé, že množství tepla potřebné k zahřátí tělesa závisí na druhu látky, ze které se těleso skládá (tedy na jeho měrné tepelné kapacitě) a na hmotnosti tělesa. Je také jasné, že množství tepla závisí na tom, o kolik stupňů se chystáme zvýšit tělesnou teplotu.
Chcete-li tedy určit množství tepla potřebného k zahřátí tělesa nebo tělesa uvolněného během chlazení, musíte vynásobit měrnou tepelnou kapacitu tělesa jeho hmotností a rozdílem mezi jeho konečnou a počáteční teplotou:
Q= cm (t 2 - t 1),
Kde Q- množství tepla, C- specifická tepelná kapacita, m- tělesná hmotnost, t 1- počáteční teplota, t 2- konečná teplota.
Když se tělo zahřeje t 2> t 1 a proto Q >0 . Když se tělo ochladí t 2i< t 1 a proto Q< 0 .
Pokud je známa tepelná kapacita celého těla S, Q určeno vzorcem: Q = C (t2 - t 1).
22) Tavení: definice, výpočet množství tepla pro tavení nebo tuhnutí, měrné skupenské teplo tání, graf t 0 (Q).
Termodynamika
Obor molekulární fyziky, který studuje přenos energie, vzorce přeměny jednoho typu energie na jiný. Na rozdíl od molekulární kinetické teorie termodynamika nebere v úvahu vnitřní struktura látek a mikroparametrů.
Termodynamický systém
Je to soubor těles, která si vyměňují energii (ve formě práce nebo tepla) mezi sebou nebo mezi sebou životní prostředí. Voda v konvici se například ochlazuje a dochází k výměně tepla mezi vodou a konvicí a teplo konvice s okolím. Válec s plynem pod pístem: píst koná práci, v důsledku čehož plyn přijímá energii a mění se jeho makroparametry.
Množství tepla
Tento energie, které systém přijímá nebo uvolňuje během procesu výměny tepla. Označuje se symbolem Q a měří se jako každá energie v joulech.
V důsledku různých procesů výměny tepla je přenášená energie určena svým vlastním způsobem.
Vytápění a chlazení
Tento proces je charakterizován změnou teploty systému. Množství tepla je určeno vzorcem

Měrná tepelná kapacita látky s měřeno množstvím tepla potřebného k zahřátí jednotky hmotnosti této látky o 1K. Ohřev 1 kg skla nebo 1 kg vody vyžaduje různé množství energie. Měrná tepelná kapacita je známá veličina, již vypočtená pro všechny látky viz hodnota ve fyzikálních tabulkách.
Tepelná kapacita látky C- to je množství tepla, které je nutné k zahřátí tělesa bez zohlednění jeho hmotnosti o 1K.


Tání a krystalizace
Tání je přechod látky z pevného do kapalného stavu. Reverzní přechod se nazývá krystalizace.
Energie, která se vynakládá na ničení krystalová mřížka látky, určené vzorcem


Měrné teplo tání je známá hodnota pro každou látku viz hodnota ve fyzikálních tabulkách.
Odpařování (odpařování nebo var) a kondenzace
Vaporizace je přechod látky z kapalného (pevného) skupenství do plynného skupenství. Opačný proces se nazývá kondenzace.


Měrné výparné teplo je známá hodnota pro každou látku viz hodnota ve fyzikálních tabulkách.
Spalování
Množství tepla uvolněného při hoření látky


Měrné spalné teplo je známá hodnota pro každou látku viz hodnota ve fyzikálních tabulkách.
Pro uzavřenou a adiabaticky izolovanou soustavu těles je splněna rovnice tepelné bilance. Algebraický součet množství tepla odevzdaného a přijatého všemi tělesy účastnícími se výměny tepla je nulové:
Q1+Q2 +...+Qn=0
23) Struktura kapalin. Povrchová vrstva. Síla povrchového napětí: příklady projevu, výpočet, koeficient povrchového napětí.
Čas od času se může jakákoli molekula přesunout na blízké volné místo. K takovým skokům v kapalinách dochází poměrně často; proto molekuly nejsou vázány na konkrétní centra, jako v krystalech, a mohou se pohybovat v celém objemu kapaliny. To vysvětluje tekutost kapalin. Díky silné interakci mezi těsně umístěnými molekulami mohou vytvářet lokální (nestabilní) uspořádané skupiny obsahující několik molekul. Tento jev se nazývá uzavřít objednávku(obr. 3.5.1).
Koeficient β se nazývá teplotní koeficient objemové roztažnosti . Tento koeficient pro kapaliny je desítkykrát větší než pro pevné látky. Pro vodu např. při teplotě 20 °C β v ≈ 2 10 – 4 K – 1, pro ocel β st ≈ 3,6 10 – 5 K – 1, pro křemenné sklo β kv ≈ 9 10 – 6 K - 1 .
Tepelná roztažnost vody má pro život na Zemi zajímavou a důležitou anomálii. Při teplotách pod 4 °C se voda s klesající teplotou rozpíná (β< 0). Максимум плотности ρ в = 10 3 кг/м 3 вода имеет при температуре 4 °С.
Když voda zamrzne, roztáhne se, takže led zůstane plavat na hladině zamrzající vodní plochy. Teplota mrznoucí vody pod ledem je 0 °C. Ve více husté vrstvy Teplota vody na dně nádrže je cca 4 °C. Díky tomu může ve vodě mrazivých nádrží existovat život.
Většina zajímavá vlastnost tekutin je přítomnost volný povrch . Kapalina na rozdíl od plynů nevyplňuje celý objem nádoby, do které se nalévá. Mezi kapalinou a plynem (nebo párou) je vytvořeno rozhraní, které je ve srovnání se zbytkem kapaliny ve zvláštních podmínkách. Je třeba mít na paměti, že vzhledem k extrémně nízké stlačitelnosti je přítomnost hustěji usazené povrchové vrstvy nevede k žádné znatelné změně objemu kapaliny. Pokud se molekula přesune z povrchu do kapaliny, síly mezimolekulární interakce vykonají pozitivní práci. Naopak, aby bylo možné vytáhnout určitý počet molekul z hloubky kapaliny na povrch (tj. zvětšit povrch kapaliny), musí vnější síly vykonat kladnou práci Δ A vnější, úměrná změně Δ S plocha povrchu:
Z mechaniky je známo, že rovnovážné stavy systému odpovídají minimální hodnotě jeho potenciální energie. Z toho vyplývá, že volný povrch kapaliny má tendenci zmenšovat svou plochu. Z tohoto důvodu má volná kapka kapaliny kulovitý tvar. Kapalina se chová tak, jako by síly působící tečně k jejímu povrchu tento povrch stahovaly (tahaly). Tyto síly se nazývají síly povrchového napětí .
Přítomnost sil povrchového napětí způsobuje, že povrch kapaliny vypadá jako elastický natažený film, pouze s tím rozdílem, že elastické síly ve filmu závisí na jeho povrchu (tj. na tom, jak je film deformován), a na povrchovém napětí. síly nezávisí na povrchu kapaliny.
Některé kapaliny, jako je mýdlová voda, mají schopnost vytvářet tenké filmy. Známé mýdlové bubliny mají pravidelný kulovitý tvar – to ukazuje i vliv sil povrchového napětí. Pokud se drátěný rám, jehož jedna strana je pohyblivá, spustí do mýdlového roztoku, pak se celý rám pokryje filmem kapaliny (obr. 3.5.3).
Síly povrchového napětí mají tendenci zmenšovat povrch fólie. Pro vyvážení pohyblivé strany rámu na ni musí působit vnější síla Pokud se pod vlivem síly příčka posune o Δ X, pak bude provedena práce Δ A vn = F vn Δ X = Δ E p = σΔ S, kde Δ S = 2LΔ X– přírůstek na povrchu obou stran mýdlového filmu. Protože moduly sil a jsou stejné, můžeme napsat:
|
Koeficient povrchového napětí σ lze tedy definovat jako modul síly povrchového napětí působící na jednotku délky čáry ohraničující povrch.
Působením sil povrchového napětí v kapkách kapaliny a uvnitř mýdlových bublin vzniká přetlak Δ p. Pokud mentálně uříznete sférický pokles poloměru R na dvě poloviny, pak každá z nich musí být v rovnováze působením sil povrchového napětí působících na hranici řezu délky 2π R a přetlakové síly působící na plochu π R 2 sekce (obr. 3.5.4). Podmínka rovnováhy se zapisuje jako
Pokud jsou tyto síly větší než síly vzájemného působení mezi molekulami samotné kapaliny, pak kapaliny mokry povrch pevné látky. V tomto případě se kapalina přibližuje k povrchu pevné látky pod určitým ostrým úhlem θ, charakteristickým pro daný pár kapalina-pevná látka. Úhel θ se nazývá kontaktní úhel . Pokud síly interakce mezi molekulami kapaliny převyšují síly jejich interakce s molekulami pevné látky, pak se kontaktní úhel θ ukáže jako tupý (obr. 3.5.5). V tomto případě říkají, že kapalina nesmáčí povrch pevné látky. Na úplné zvlhčeníθ = 0, at úplné nesmáčení 6 = 180°.
Kapilární jevy nazývá se vzestup nebo pokles kapaliny v trubkách malého průměru - kapiláry. Smáčecí kapaliny stoupají kapilárami, nesmáčivé kapaliny sestupují.
Na Obr. 3.5.6 ukazuje kapiláru o určitém poloměru r, spuštěný na spodním konci do smáčecí kapaliny o hustotě ρ. Horní konec kapiláry je otevřený. Vzestup kapaliny v kapiláře pokračuje, dokud gravitační síla působící na sloupec kapaliny v kapiláře nebude mít stejnou velikost jako výslednice F n Síly povrchového napětí působící podél hranice kontaktu kapaliny s povrchem kapiláry: F t = F n, kde F t = mg = ρ hπ r 2 G, F n = σ2π r cos θ.
Z toho vyplývá:
Při úplném nesmáčení θ = 180° je cos θ = –1, a proto h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Voda téměř úplně smáčí čistý skleněný povrch. Naopak rtuť zcela nesmáčí povrch skla. Hladina rtuti ve skleněné kapiláře proto klesá pod hladinu v nádobě.
24) Vaporizace: definice, druhy (odpařování, var), výpočet množství tepla pro vypařování a kondenzaci, měrné teplo vypařování.
Odpařování a kondenzace. Vysvětlení jevu vypařování na základě představ o molekulární struktuře hmoty. Měrné výparné teplo. Její jednotky.
Jev přeměny kapaliny na páru se nazývá vypařování.
Vypařování - proces odpařování probíhající z otevřeného povrchu.
Molekuly kapaliny se pohybují s při různých rychlostech. Pokud nějaká molekula skončí na povrchu kapaliny, může překonat přitažlivost sousedních molekul a vyletět z kapaliny. Vyvržené molekuly tvoří páru. Zbývající molekuly kapaliny při srážce mění rychlost. Některé molekuly přitom získávají rychlost dostatečnou k vylétnutí z kapaliny. Tento proces pokračuje, takže se kapaliny pomalu odpařují.
*Rychlost odpařování závisí na typu kapaliny. Ty kapaliny, jejichž molekuly jsou přitahovány menší silou, se odpařují rychleji.
* K odpařování může dojít při jakékoli teplotě. Ale při vysokých teplotách dochází k odpařování rychleji .
*Rychlost odpařování závisí na jeho povrchu.
*Při větru (proudění vzduchu) dochází k rychlejšímu odpařování.
Při vypařování se vnitřní energie snižuje, protože Během odpařování kapalina opouští rychlé molekuly, proto průměrná rychlost počet zbývajících molekul klesá. To znamená, že pokud nedochází k přílivu energie zvenčí, pak teplota kapaliny klesá.
 Jev přeměny páry v kapalinu se nazývá kondenzace.
Je doprovázena uvolňováním energie.
Jev přeměny páry v kapalinu se nazývá kondenzace.
Je doprovázena uvolňováním energie.
Kondenzace páry vysvětluje vznik mraků. Vodní pára stoupající nad zemí tvoří v horních studených vrstvách vzduchu mraky, které se skládají z drobných kapiček vody.
Měrné výparné teplo - fyzický hodnota ukazující, kolik tepla je potřeba k přeměně kapaliny o hmotnosti 1 kg na páru beze změny teploty.
Ud. výparné teplo označeno písmenem L a měřeno v J/kg
Ud. výparné teplo vody: L=2,3×106 J/kg, alkohol L=0,9×106
Množství tepla potřebné k přeměně kapaliny na páru: Q = Lm
Jak je známo, během různých mechanických procesů dochází ke změně mechanické energie. Měřítkem změny mechanické energie je práce sil působících na systém:
Při výměně tepla dochází ke změně vnitřní energie těla. Měřítkem změny vnitřní energie při přenosu tepla je množství tepla.
Množství tepla je míra změny vnitřní energie, kterou tělo přijímá (nebo se vzdává) během procesu výměny tepla.
Práce i množství tepla tedy charakterizují změnu energie, ale nejsou totožné s energií. Necharakterizují stav samotného systému, ale určují proces energetického přechodu z jednoho typu do druhého (z jednoho tělesa do druhého), kdy se stav mění a výrazně závisí na povaze procesu.
Hlavní rozdíl mezi prací a množstvím tepla je v tom, že práce charakterizuje proces změny vnitřní energie systému, doprovázený přeměnou energie z jednoho typu na druhý (z mechanické na vnitřní). Množství tepla charakterizuje proces přenosu vnitřní energie z jednoho tělesa do druhého (od více zahřátého k méně zahřátému), neprovázený energetickými přeměnami.
Zkušenosti ukazují, že množství tepla potřebné k ohřátí tělesa o hmotnosti m z teploty na teplotu se vypočítá podle vzorce
kde c je měrná tepelná kapacita látky;
![]()
Jednotkou SI měrné tepelné kapacity je joule na kilogram Kelvina (J/(kg K)).
Specifické teplo c se číselně rovná množství tepla, které musí být předáno tělesu o hmotnosti 1 kg, aby se zahřálo o 1 K.
Tepelná kapacita těleso se číselně rovná množství tepla potřebného ke změně tělesné teploty o 1 K:
![]()
Jednotkou SI tepelné kapacity tělesa je joule na Kelvin (J/K).
K přeměně kapaliny na páru při konstantní teplotě je nutné vydat určité množství tepla
kde L je měrné skupenské teplo vypařování. Při kondenzaci páry se uvolňuje stejné množství tepla.
730. Proč se voda používá k chlazení některých mechanismů?
Voda má vysokou měrnou tepelnou kapacitu, což usnadňuje dobrý odvod tepla z mechanismu.
731. V jakém případě je třeba vynaložit více energie: ohřát jeden litr vody o 1 °C nebo ohřát sto gramů vody o 1 °C?
Na zahřátí litru vody platí, že čím větší hmotnost, tím více energie je třeba vynaložit.
732. Stříbrné a stříbrné vidličky z kupronickelu o stejné hmotnosti byly spuštěny do horké vody. Dostanou stejné množství tepla z vody?
Kuproniklová vidlička obdrží více tepla, protože měrné teplo měďnatého niklu je větší než stříbra.
733. Kousek olova a kus litiny o stejné hmotnosti byly třikrát udeřeny perlíkem. Který kousek byl teplejší?
Olovo se zahřeje, protože jeho specifická tepelná kapacita je nižší než u litiny a zahřátí olova vyžaduje méně energie.
734. Jedna baňka obsahuje vodu, druhá petrolej o stejné hmotnosti a teplotě. Do každé baňky byla vhozena stejně zahřátá železná kostka. Co se zahřeje na více vysoká teplota– voda nebo petrolej?
Petrolej.
735. Proč jsou teplotní výkyvy v zimě a v létě méně výrazné ve městech na pobřeží než ve městech ve vnitrozemí?
Voda se ohřívá a ochlazuje pomaleji než vzduch. V zimě se ochladí a hýbe se teplé masy vzduchu na pevninu, čímž se klima na pobřeží otepluje.
736. Měrná tepelná kapacita hliníku je 920 J/kg °C. Co to znamená?
To znamená, že na ohřátí 1 kg hliníku o 1 °C je potřeba vynaložit 920 J.
737. Hliníkové a měděné tyče o stejné hmotnosti 1 kg se ochladí o 1 °C. Jak moc se změní vnitřní energie každého bloku? U které lišty se to změní více a o kolik?
738. Jaké množství tepla je potřeba k ohřátí kilogramu železného předvalku o 45 °C?

739. Jaké množství tepla je potřeba k ohřevu 0,25 kg vody z 30 °C na 50 °C?
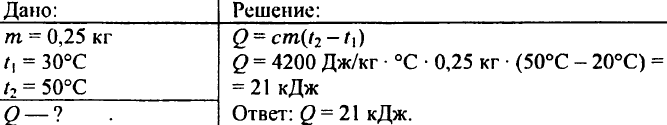
740. Jak se změní vnitřní energie dvou litrů vody při zahřátí o 5 °C?

741. Jaké množství tepla je potřeba k ohřevu 5 g vody z 20 °C na 30 °C?

742. Jaké množství tepla je potřeba k zahřátí hliníkové koule o hmotnosti 0,03 kg na 72 °C?

743. Vypočítejte množství tepla potřebného k ohřevu 15 kg mědi o 80 °C.

744. Vypočítejte množství tepla potřebného k ohřevu 5 kg mědi z 10 °C na 200 °C.

745. Jaké množství tepla je potřeba k ohřevu 0,2 kg vody z 15 °C na 20 °C?

746. Voda o hmotnosti 0,3 kg se ochladila o 20 °C. Jak moc se snížila vnitřní energie vody?

747. Jaké množství tepla je potřeba k ohřevu 0,4 kg vody o teplotě 20 °C na teplotu 30 °C?

748. Jaké množství tepla je vynaloženo na ohřátí 2,5 kg vody o 20 °C?

749. Jaké množství tepla se uvolnilo při ochlazení 250 g vody z 90 °C na 40 °C?

750. Jaké množství tepla je potřeba k ohřátí 0,015 litru vody o 1 °C?

751. Vypočítejte množství tepla potřebného k ohřevu jezírka o objemu 300 m3 o 10 °C?

752. Jaké množství tepla je třeba přidat k 1 kg vody, aby se její teplota zvýšila z 30 °C na 40 °C?

753. Voda o objemu 10 litrů se zchladila z teploty 100 °C na teplotu 40 °C. Kolik tepla se během toho uvolnilo?

754. Vypočítejte množství tepla potřebného k ohřátí 1 m3 písku o 60 °C.

755. Objem vzduchu 60 m3, měrná tepelná kapacita 1000 J/kg °C, hustota vzduchu 1,29 kg/m3. Kolik tepla je potřeba ke zvýšení teploty na 22 °C?

756. Voda se zahřála o 10 °C, přičemž se spotřebovalo 4,20 ± 103 J tepla. Určete množství vody.

757. Vodě o hmotnosti 0,5 kg bylo předáno 20,95 kJ tepla. Jaká byla teplota vody, když byla počáteční teplota vody 20 °C?

758. Měděná pánev o hmotnosti 2,5 kg se naplní 8 kg vody o teplotě 10 °C. Kolik tepla je potřeba k ohřevu vody v pánvi k varu?

759. Do měděné naběračky o hmotnosti 300 g se nalije litr vody o teplotě 15 °C Jaké množství tepla je potřeba k ohřevu vody v naběračce na 85 °C?

760. Kus rozehřáté žuly o hmotnosti 3 kg se vloží do vody. Žula předá vodě 12,6 kJ tepla, chlazení o 10 °C. Jaká je měrná tepelná kapacita kamene?

761. Horká voda o teplotě 50 °C byla přidána k 5 kg vody o teplotě 12 °C, čímž byla získána směs o teplotě 30 °C. Kolik vody jsi přidal?

762. Voda o teplotě 20 °C byla přidána do 3 litrů vody o teplotě 60 °C, čímž byla získána voda o teplotě 40 °C. Kolik vody jsi přidal?

763. Jaká bude teplota směsi, smícháte-li 600 g vody 80 °C s 200 g vody 20 °C?

764. Litr vody o teplotě 90 °C byl nalit do vody o teplotě 10 °C a teplota vody dosáhla 60 °C. Kolik jich bylo studená voda?

765. Určete, kolik nalít do nádoby horká voda, zahřátý na 60 °C, pokud nádoba již obsahuje 20 litrů studené vody o teplotě 15 °C; teplota směsi by měla být 40 °C.

766. Určete, kolik tepla je potřeba k ohřevu 425 g vody o 20 °C.

767. O kolik stupňů se ohřeje 5 kg vody, pokud voda přijme 167,2 kJ?

768. Kolik tepla je potřeba k ohřevu m gramů vody o teplotě t1 na teplotu t2?
769. 2 kg vody se nalije do kalorimetru o teplotě 15 °C. Na jakou teplotu se ohřeje voda v kalorimetru, když se do ní spustí 500g mosazné závaží zahřáté na 100 °C? Měrná tepelná kapacita mosazi je 0,37 kJ/(kg °C).

770. Existují kusy mědi, cínu a hliníku stejného objemu. Který z těchto kusů má největší a který nejmenší tepelnou kapacitu?

771. Do kalorimetru bylo nalito 450 g vody, jejíž teplota byla 20 °C. Když bylo do této vody ponořeno 200 g železných pilin zahřátých na 100 °C, teplota vody dosáhla 24 °C. Určete měrnou tepelnou kapacitu pilin.

772. Měděný kalorimetr o hmotnosti 100 g pojme 738 g vody, jejíž teplota je 15 °C. Do tohoto kalorimetru bylo zapuštěno 200 g mědi při teplotě 100 °C, načež teplota kalorimetru stoupla na 17 °C. Jaká je měrná tepelná kapacita mědi?
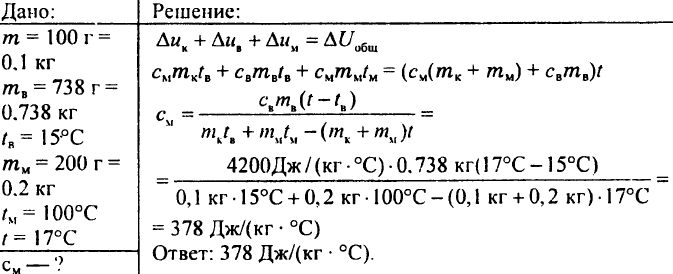
773. Ocelová kulička o hmotnosti 10 g se vyjme z pece a vloží se do vody o teplotě 10 °C. Teplota vody stoupla na 25 °C. Jaká byla teplota koule v troubě, když hmotnost vody byla 50 g? Měrná tepelná kapacita oceli je 0,5 kJ/(kg °C).

777. 50 g vody o teplotě 19 °C bylo nalito do vody o hmotnosti 150 g o teplotě 35 °C. Jaká je teplota směsi?

778. Do litinového hrnce o hmotnosti 2 kg o teplotě 10 °C byla nalita voda o hmotnosti 5 kg o teplotě 90 °C. Jaká byla teplota vody?

779. Ocelový řezák o hmotnosti 2 kg byl zahřát na teplotu 800 °C a poté spuštěn do nádoby obsahující 15 litrů vody o teplotě 10 °C. Na jakou teplotu se ohřeje voda v nádobě?

(Indikace: Pro vyřešení tohoto problému je nutné vytvořit rovnici, ve které se neznámá teplota bere jako neznámá teplota vody v nádobě po spuštění řezačky.)
780. Jakou teplotu získá voda, když smícháte 0,02 kg vody o teplotě 15 °C, 0,03 kg vody o teplotě 25 °C a 0,01 kg vody o teplotě 60 °C?

781. Pro vytápění dobře větrané třídy je potřebné množství tepla 4,19 MJ za hodinu. Voda vstupuje do radiátorů o teplotě 80 °C a opouští je při teplotě 72 °C. Kolik vody by se mělo dodávat do radiátorů každou hodinu?

782. Olovo o hmotnosti 0,1 kg o teplotě 100 °C bylo ponořeno do hliníkového kalorimetru o hmotnosti 0,04 kg obsahujícího 0,24 kg vody o teplotě 15 °C. Poté teplota v kalorimetru dosáhla 16 °C. Jaké je měrné teplo olova?

VÝMĚNA TEPLA.
1. Přenos tepla.
Tepelná výměna nebo přenos tepla je proces přenosu vnitřní energie jednoho těla do druhého bez vykonávání práce.
Existují tři typy přenosu tepla.
1) Tepelná vodivost- Jedná se o výměnu tepla mezi tělesy při jejich přímém kontaktu.
2) Proudění- Jedná se o výměnu tepla, při které se teplo přenáší proudy plynu nebo kapaliny.
3) Záření– Jedná se o výměnu tepla prostřednictvím elektromagnetického záření.
2. Množství tepla.
Množství tepla je mírou změny vnitřní energie tělesa při výměně tepla. Označeno písmenem Q.
Jednotka pro měření množství tepla = 1 J.
Množství tepla přijaté tělesem od jiného tělesa v důsledku výměny tepla může být vynaloženo na zvýšení teploty (zvýšení kinetické energie molekul) nebo změnu stavu agregace (zvýšení potenciální energie).
3.Měrná tepelná kapacita látky.
Zkušenost ukazuje, že množství tepla potřebné k ohřátí tělesa o hmotnosti m z teploty T 1 na teplotu T 2 je úměrné hmotnosti tělesa m a rozdílu teplot (T 2 - T 1), tzn.
Q = cm(T 2 - T 1 ) = smΔ T,
S se nazývá měrná tepelná kapacita látky ohřívaného tělesa.
![]()
Měrná tepelná kapacita látky se rovná množství tepla, které se musí předat 1 kg látky, aby se zahřála o 1 K.
Jednotka měření měrné tepelné kapacity =.
Hodnoty tepelné kapacity pro různé látky lze nalézt ve fyzikálních tabulkách.
Přesně stejné množství tepla Q se uvolní, když se těleso ochladí o ΔT.
4.Měrné výparné teplo.
Zkušenosti ukazují, že množství tepla potřebného k přeměně kapaliny na páru je úměrné hmotnosti kapaliny, tzn.
Q = Lm,
kde je koeficient proporcionality L volal specifické teplo vypařování.
Měrné výparné teplo se rovná množství tepla potřebného k přeměně 1 kg kapaliny při bodu varu na páru.
Jednotka měření měrného výparného tepla.
Při zpětném procesu, kondenzaci páry, se uvolňuje teplo ve stejném množství, jaké bylo vynaloženo na tvorbu páry.
5.Specifické teplo tání.
Zkušenosti ukazují, že množství tepla potřebného k přeměně pevný do kapaliny, úměrně tělesné hmotnosti, tzn.
Q = λ m,
kde koeficient úměrnosti λ se nazývá měrné teplo tání.
Měrné teplo tání se rovná množství tepla, které je nutné k přeměně pevného tělesa o hmotnosti 1 kg na kapalinu při teplotě tání.
Jednotka měření měrného tepla tání.
Během reverzního procesu, krystalizace kapaliny, se uvolňuje teplo ve stejném množství, jaké bylo vynaloženo na tavení.
6. Měrné spalné teplo.
Zkušenosti ukazují, že množství tepla uvolněného při úplném spálení paliva je úměrné hmotnosti paliva, tzn.
Q = qm,
Kde koeficient úměrnosti q se nazývá měrné spalné teplo.
Měrné spalné teplo se rovná množství tepla uvolněného při úplném spálení 1 kg paliva.
Jednotka měření měrného spalného tepla.
7. Rovnice tepelné bilance.
Výměna tepla se týká dvou nebo více těles. Některá tělesa teplo vydávají, jiná ho přijímají. K výměně tepla dochází, dokud se teploty těles nevyrovnají. Podle zákona zachování energie se množství tepla, které se vydává, rovná množství, které je přijato. Na tomto základě je napsána rovnice tepelné bilance.
Podívejme se na příklad.
Těleso o hmotnosti m 1, jehož tepelná kapacita je c 1, má teplotu T 1 a těleso o hmotnosti m 2, jehož tepelná kapacita je c 2, má teplotu T 2. Navíc Ti je větší než T2. Tato těla jsou uvedena do kontaktu. Zkušenosti ukazují, že studené těleso (m 2) se začne ohřívat a horké těleso (m 1) se začne ochlazovat. To naznačuje, že část vnitřní energie horkého tělesa se přenese na studené a teploty se vyrovnají. Označme výslednou celkovou teplotu θ. 
Množství tepla přeneseného z horkého tělesa na studené
Q přestoupil. = C 1 m 1 (T 1 – θ )
Množství tepla přijatého studeným tělesem od horkého
Q přijaté. = C 2 m 2 (θ – T 2 )
Podle zákona zachování energie Q přestoupil. = Q přijaté., tj.
C 1 m 1 (T 1 – θ )= C 2 m 2 (θ – T 2 )
Otevřeme závorky a vyjádříme hodnotu celkové ustálené teploty θ.
![]()
V tomto případě získáme hodnotu teploty θ v kelvinech.
Protože se však Q předává ve výrazech. a Q je přijato. je rozdíl mezi dvěma teplotami a je stejný jak v Kelvinech, tak ve stupních Celsia, pak lze výpočet provést ve stupních Celsia. Pak
![]()
V tomto případě získáme hodnotu teploty θ ve stupních Celsia.
Vyrovnání teplot v důsledku tepelné vodivosti lze na základě molekulární kinetické teorie vysvětlit jako výměnu kinetické energie mezi molekulami při srážce v procesu tepelného chaotického pohybu.
Tento příklad lze ilustrovat grafem. 
V této lekci se naučíme, jak vypočítat množství tepla potřebného k zahřátí tělesa nebo tělesa uvolněného při ochlazování. K tomu si shrneme znalosti, které jsme získali v předchozích lekcích.
Kromě toho se naučíme pomocí vzorce pro množství tepla vyjádřit z tohoto vzorce zbývající veličiny a vypočítat je se znalostí jiných veličin. Bude také zvažován příklad problému s řešením výpočtu množství tepla.
Tato lekce je věnována výpočtu množství tepla, když se těleso zahřívá nebo uvolňuje při ochlazení.
Schopnost vypočítat potřebné množství tepla je velmi důležitá. To může být potřeba například při výpočtu množství tepla, které je třeba předat vodě k vytápění místnosti.
Rýže. 1. Množství tepla, které musí být předáno vodě, aby se místnost vytopila
Nebo pro výpočet množství tepla, které se uvolňuje při spalování paliva v různých motorech:

Rýže. 2. Množství tepla, které se uvolňuje při spalování paliva v motoru
Tyto znalosti jsou také potřeba například k určení množství tepla, které se uvolňuje Sluncem a dopadá na Zemi:

Rýže. 3. Množství tepla uvolněného Sluncem a dopadajícího na Zemi
Pro výpočet množství tepla potřebujete vědět tři věci (obr. 4):
- tělesná hmotnost (kterou lze obvykle měřit pomocí váhy);
- teplotní rozdíl, o který se musí těleso zahřát nebo ochladit (obvykle měřeno teploměrem);
- měrná tepelná kapacita tělesa (kterou lze určit z tabulky).

Rýže. 4. Co potřebujete vědět k určení
Vzorec, podle kterého se vypočítá množství tepla, vypadá takto:
V tomto vzorci se objevují následující množství:
množství tepla měřené v joulech (J);
Měrná tepelná kapacita látky se měří v ;
- teplotní rozdíl, měřený ve stupních Celsia ().
Zvažme problém výpočtu množství tepla.
Úkol
Měděné sklo o hmotnosti gramů obsahuje vodu o objemu litrů při teplotě. Kolik tepla se musí předat sklenici vody, aby se její teplota vyrovnala ?

Rýže. 5. Ilustrace problémových stavů
Nejprve si zapíšeme krátkou podmínku ( Dáno) a převést všechny veličiny na mezinárodní systém (SI).
|
Vzhledem k tomu: |
SI |
|
|
Nalézt: |
Řešení:
Nejprve určete, jaké další veličiny potřebujeme k vyřešení tohoto problému. Pomocí tabulky měrné tepelné kapacity (tabulka 1) zjistíme (měrnou tepelnou kapacitu mědi, protože podle stavu je sklo měď), (měrnou tepelnou kapacitu vody, protože podle podmínek je ve skle voda). Navíc víme, že k výpočtu množství tepla potřebujeme hmotnost vody. Podle stavu nám je dán pouze objem. Proto z tabulky vezmeme hustotu vody: (Tabulka 2).
Stůl 1. Měrná tepelná kapacita některých látek,
Stůl 2. Hustoty některých kapalin
Nyní máme vše, co k vyřešení tohoto problému potřebujeme.
Všimněte si, že konečné množství tepla se bude skládat ze součtu množství tepla potřebného k ohřevu měděného skla a množství tepla potřebného k ohřevu vody v něm:
Nejprve spočítejme množství tepla potřebného k ohřevu měděného skla:
Před výpočtem množství tepla potřebného k ohřevu vody vypočítejme hmotnost vody pomocí vzorce, který je nám známý ze třídy 7:
Nyní můžeme počítat:
Pak můžeme počítat:
Připomeňme si, co znamenají kilojouly. Předpona "kilo" znamená ![]() .
.
Odpovědět:.
Pro usnadnění řešení problémů zjišťování množství tepla (tzv. přímé problémy) a množství spojených s tímto pojmem můžete použít následující tabulku.
|
Požadované množství |
Označení |
Jednotky |
Základní vzorec |
Vzorec pro množství |
|
Množství tepla |
